Ioniske forbindelser:Forståelse af kemiske formler og krystalstrukturer
* Ioniske forbindelser danner ikke molekyler. De danner krystalgitre, hvor positive og negative ioner holdes sammen af elektrostatisk tiltrækning i et fast forhold.
* Formlen repræsenterer det enkleste hele talforhold mellem ioner i forbindelsen. Det viser ikke det faktiske arrangement eller antallet af ioner i krystalstrukturen.
Eksempel:
* NaCl (natriumchlorid) :Formlen viser én natriumion (Na+) for hver chloridion (Cl-). Det fortæller dig ikke, hvor mange natrium- eller chloridioner, der er til stede i en bestemt krystal.
I modsætning hertil danner kovalente forbindelser molekyler, og deres kemiske formler repræsenterer det faktiske antal og typer af atomer i et enkelt molekyle.
Eksempel:
* H2O (vand): Formlen viser, at et vandmolekyle indeholder to brintatomer og et oxygenatom.
Sidste artikelForståelse af 9-kulstofkulhydrater:formler og strukturer
Næste artikelIoniske forbindelser:Forståelse af formler og struktur
 Varme artikler
Varme artikler
-
 Ekspertvejledning:Adskillelse af alkohol fra vand via fraktioneret destillationAf Yasho Raval Opdateret 24. marts 2022 For at adskille en blanding af alkohol (ethanol) og vand, kan du bruge en proces kendt som fraktioneret destillation. Denne teknik er afhængig af, at forbinde
Ekspertvejledning:Adskillelse af alkohol fra vand via fraktioneret destillationAf Yasho Raval Opdateret 24. marts 2022 For at adskille en blanding af alkohol (ethanol) og vand, kan du bruge en proces kendt som fraktioneret destillation. Denne teknik er afhængig af, at forbinde -
 Ren teknologi til fremstilling af lavmolekylær chitosanPlasma-assisteret depolymerisation af chitosan i en kvartsblandingsanordning. Kredit:MIPT Forskere ved MIPT har udviklet en ny teknik til at opnå lavmolekylær vægt, vandopløseligt kitin og chitosa
Ren teknologi til fremstilling af lavmolekylær chitosanPlasma-assisteret depolymerisation af chitosan i en kvartsblandingsanordning. Kredit:MIPT Forskere ved MIPT har udviklet en ny teknik til at opnå lavmolekylær vægt, vandopløseligt kitin og chitosa -
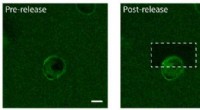 Forskere bruger molekylære tether og kemiske lyssabler til at konstruere platforme til vævsteknikFotofrigivelse af proteiner fra epidermal vækstfaktor (EGF) på den ene side af en human celle. Til venstre:EGF (grøn) er bundet til en hydrogel en enkelt menneskelig celle (i midten). Cellemembranen b
Forskere bruger molekylære tether og kemiske lyssabler til at konstruere platforme til vævsteknikFotofrigivelse af proteiner fra epidermal vækstfaktor (EGF) på den ene side af en human celle. Til venstre:EGF (grøn) er bundet til en hydrogel en enkelt menneskelig celle (i midten). Cellemembranen b -
 Ny teknik til at studere rustning af stål gavner mineindustrienArthur Situm ved den canadiske lyskildesynkrotron. Kredit:Dave Stobbe University of Saskatchewan (USask) Ph.D. studerende Arthur Situm har udviklet en ny ikke-invasiv teknik til at studere rusten
Ny teknik til at studere rustning af stål gavner mineindustrienArthur Situm ved den canadiske lyskildesynkrotron. Kredit:Dave Stobbe University of Saskatchewan (USask) Ph.D. studerende Arthur Situm har udviklet en ny ikke-invasiv teknik til at studere rusten
- Hvordan bliver DNA'et i cellelysat synligt?
- Hvor sikker er nanoteknologiforskning i Sydøstasien?
- Hvilken ledning bruger Tom Hill skulpturen?
- Forskerhold udpeger kilden til den unikke kemiske sammensætning af vulkanske klipper
- Hvad er reaktionen, der finder sted mellem bly- og sølvnitrat?
- Hvilken kraft kan tænkes som enten et skub eller træk længe, det får objektet til at bevæge s…


