Krystalstrukturer af NaCl og MgO:En detaljeret analyse
Struktur af natriumchlorid (NaCl) og magnesiumoxid (MgO) som faste stoffer:
Både natriumchlorid (NaCl) og magnesiumoxid (MgO) er ioniske forbindelser med en krystalgitterstruktur . Dette betyder, at deres bestanddele er arrangeret i et meget ordnet, gentaget mønster.
Natriumchlorid (NaCl):
* Krystalstruktur: Ansigtscentreret kubisk (FCC) gitter.
* Ionisk arrangement: Natriumkationer (Na+) og chloridanioner (Cl-) veksler i forholdet 1:1. Forestil dig et 3D-skakternmønster, hvor hver ion er omgivet af seks ioner med den modsatte ladning.
* Binding: Stærk elektrostatisk tiltrækning mellem modsat ladede ioner.
* Egenskaber: Høje smelte- og kogepunkter, hård og skør, opløselig i vand.
Magnesiumoxid (MgO):
* Krystalstruktur: Svarende til NaCl, med et ansigtscentreret kubisk gitter.
* Ionisk arrangement: Magnesiumkationer (Mg2+) og oxidanioner (O2-) veksler i forholdet 1:1. Arrangementet er dog lidt anderledes end NaCl på grund af ionernes forskellige ladninger.
* Binding: Endnu stærkere elektrostatisk tiltrækning end i NaCl på grund af ionernes højere ladninger.
* Egenskaber: Meget høje smelte- og kogepunkter, ekstremt hård og skør, uopløselig i vand.
Ligheder:
* Begge har kubiske krystalstrukturer.
* Begge er ioniske forbindelser med stærke elektrostatiske kræfter, der holder dem sammen.
* Begge har høje smelte- og kogepunkter på grund af de stærke ionbindinger.
Forskelle:
* Ionernes størrelse: Mg2+ og O2- er mindre end Na+ og Cl-, hvilket fører til en tættere pakning i MgO.
* Ladning af ioner: Mg2+ og O2- har højere ladninger end Na+ og Cl-, hvilket resulterer i stærkere elektrostatiske kræfter og højere smeltepunkt i MgO.
* Opløselighed: NaCl er opløseligt i vand, mens MgO er uopløseligt.
Sammenfattende har både NaCl og MgO lignende krystalstrukturer, men forskellene i ionstørrelse og ladning fører til forskellige egenskaber, især med hensyn til smeltepunkt og opløselighed.
 Varme artikler
Varme artikler
-
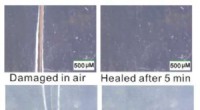 Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft
Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft -
 Undersøgelsesresultater baner vejen for programmerbare elektroniske blækMengmeng Li og René Janssen. Kredit:Eindhoven University of Technology Konjugerede polymerer er vigtige materialer på grund af deres specielle elektroniske og optiske egenskaber og lave omkostning
Undersøgelsesresultater baner vejen for programmerbare elektroniske blækMengmeng Li og René Janssen. Kredit:Eindhoven University of Technology Konjugerede polymerer er vigtige materialer på grund af deres specielle elektroniske og optiske egenskaber og lave omkostning -
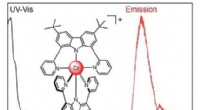 Et nyt kromkompleks udsender lys i uhåndgribelig NIR-II-bølgelængdeKredit:Wiley Mange applikationer, fra fiberoptisk telekommunikation til biomedicinske billeddannelsesprocesser kræver stoffer, der udsender lys i det nær-infrarøde område (NIR). Et forskerhold i S
Et nyt kromkompleks udsender lys i uhåndgribelig NIR-II-bølgelængdeKredit:Wiley Mange applikationer, fra fiberoptisk telekommunikation til biomedicinske billeddannelsesprocesser kræver stoffer, der udsender lys i det nær-infrarøde område (NIR). Et forskerhold i S -
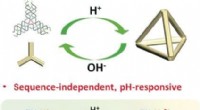 Universel pH-reguleret samling af DNA-nanostrukturerDNA, bæreren af genetisk information, er blevet etableret som et yderst anvendeligt byggemateriale inden for nanoteknologi. Et krav i mange applikationer er den kontrollerede, omskiftelig samling af
Universel pH-reguleret samling af DNA-nanostrukturerDNA, bæreren af genetisk information, er blevet etableret som et yderst anvendeligt byggemateriale inden for nanoteknologi. Et krav i mange applikationer er den kontrollerede, omskiftelig samling af
- Er det sandt, at et mål for den kinetiske energipartikelbevægelse inden for et stof er temperatur?…
- Hvad er hypotesen om en tornado i krukke til videnskabsprojekt?
- Er homogene blandingspartikler spredt jævnt?
- Hvad er de 5 egenskaber ved kemisk forandring?
- Hvad producerer planter i den første fase af fotosyntesen?
- Mægtige flod, mægtigt filter:Gendannet flodslette hjælper med at helbrede Mississippi-floden


