Forståelse af oxidationstallet for nitrogen i hydrazin (N₂H₄)
Forståelse af oxidationstal
* Oxidationstal er en måde at holde styr på elektronerne i et molekyle eller ion. De repræsenterer den hypotetiske ladning et atom ville have, hvis alle bindingerne var ioniske.
* Regler for tildeling af oxidationsnumre:
* Oxidationstallet for et grundstof i dets grundstofform er 0.
* Oxidationstallet for en monoatomisk ion er lig med dens ladning.
* Oxidationstallet for oxygen i de fleste forbindelser er -2 (undtagen i peroxider, hvor det er -1).
* Oxidationstallet for brint i de fleste forbindelser er +1 (undtagen i metalhydrider, hvor det er -1).
* Summen af oxidationstallene i et neutralt molekyle er 0.
* Summen af oxidationstallene i en polyatomisk ion er lig med ladningen af ionen.
Anvendelse af reglerne på hydrazin (N₂H₄):
1. Brints oxidationstal: I hydrazin er hydrogen bundet til nitrogen, så dets oxidationstal er +1.
2. Lad x være oxidationstallet for nitrogen: Da der er to nitrogenatomer i hydrazin, er det samlede oxidationstal for nitrogen 2x.
3. Summen af oxidationstal: Summen af oxidationstallene i hydrazin skal være lig nul:2x + 4(+1) =0
4. Løs for x: 2x + 4 =0 => 2x =-4 => x =-2
Derfor er oxidationstallet for nitrogen i hydrazin -2.
 Varme artikler
Varme artikler
-
 Syntetiske brændstoffer kan mindske CO2-fodaftrykketKredit:CC0 Public Domain Syntetiske brændstoffer, lavet ved hjælp af kulstof fanget fra luften, landbrugsaffald eller biomasse, kunne hjælpe transportsektoren med at reducere sin afhængighed af fo
Syntetiske brændstoffer kan mindske CO2-fodaftrykketKredit:CC0 Public Domain Syntetiske brændstoffer, lavet ved hjælp af kulstof fanget fra luften, landbrugsaffald eller biomasse, kunne hjælpe transportsektoren med at reducere sin afhængighed af fo -
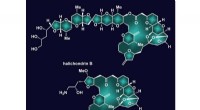 Tilbagevendelse fremskynder oprettelsen af et vigtigt molekyle:Lab gør syntesen af halichondrin…Rice University syntetiske kemikere har forenklet processen med at lave halichondrin B, top, moderforbindelsen til det succesfulde kræftlægemiddel eribulin, bund. Deres omvendte syntese reducerede ant
Tilbagevendelse fremskynder oprettelsen af et vigtigt molekyle:Lab gør syntesen af halichondrin…Rice University syntetiske kemikere har forenklet processen med at lave halichondrin B, top, moderforbindelsen til det succesfulde kræftlægemiddel eribulin, bund. Deres omvendte syntese reducerede ant -
 Undersøgelse afdækker ny hindring for udvikling af immunterapierBrian Baker, John A. Zahm, C.S.C., Professor i strukturbiologi og formand for Institut for Kemi og Biokemi Kredit:University of Notre Dame Kroppens immunsystem er et tappert våben mod sygdom, og u
Undersøgelse afdækker ny hindring for udvikling af immunterapierBrian Baker, John A. Zahm, C.S.C., Professor i strukturbiologi og formand for Institut for Kemi og Biokemi Kredit:University of Notre Dame Kroppens immunsystem er et tappert våben mod sygdom, og u -
 Detektering af ethylen, frugtmodningshormonetFigur viser den potentielle anvendelse af anvendelse af fluorescerende sonde til påvisning af ethylengas under modningsprocesser af frugter. I nærvær af ethylengas, fluoroforerne i proberne aktiveres
Detektering af ethylen, frugtmodningshormonetFigur viser den potentielle anvendelse af anvendelse af fluorescerende sonde til påvisning af ethylengas under modningsprocesser af frugter. I nærvær af ethylengas, fluoroforerne i proberne aktiveres


