Hvilke stoffer skaber grundlæggende løsninger? En omfattende guide
* Grundlæggende løsninger: Basisopløsninger har en pH-værdi på mere end 7. De er også kendt som alkaliske opløsninger.
Lad os analysere hver mulighed:
* A. Ammoniumnitrit (NH₄NO₂): Dette salt vil producere en let sur opløsning. Ammoniumioner (NH4⁺) er svagt sure, mens nitritioner (NO₂⁻) er svagt basiske. Den sure natur af ammoniumioner dominerer i dette tilfælde.
* B. Salpetersyrling (HNO₂): Dette er en svag syre. Det vil producere en sur opløsning.
* C. Natriumacetat (CH₃COONa): Dette salt vil producere en basisk opløsning. Acetationer (CH₃COO⁻) er den konjugerede base af en svag syre (eddikesyre, CH₃COOH), hvilket gør dem svagt basiske.
* D. NaCl (natriumchlorid): Dette er et neutralt salt. Det dannes ved reaktion af en stærk syre (HCl) og en stærk base (NaOH), hvilket resulterer i en neutral opløsning.
* E. Jodid (I⁻): Jodidioner er den konjugerede base af en stærk syre (HI). Selvom de teknisk set er en base, er de meget svage og vil ikke påvirke pH væsentligt, hvilket resulterer i en neutral opløsning.
* F. Hydroxid (OH⁻): Hydroxidioner er den definerende karakteristik af baser. De accepterer let protoner (H⁺), hvilket gør opløsninger, der indeholder dem, stærkt basiske.
Derfor er de stoffer, der producerer basisopløsninger:
* C. Natriumacetat (CH₃COONa)
* F. Hydroxid (OH⁻)
Sig til, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
 Forskere finder en ny opbevaringsmekanisme for opladningKredit:Pixabay/CC0 Public Domain Forskning mellem University of Liverpool, Storbritannien og National Tsing Hua University (NTHU), Taiwan har afsløret en ny opladningsmekanisme, der har potentiale
Forskere finder en ny opbevaringsmekanisme for opladningKredit:Pixabay/CC0 Public Domain Forskning mellem University of Liverpool, Storbritannien og National Tsing Hua University (NTHU), Taiwan har afsløret en ny opladningsmekanisme, der har potentiale -
 En miljøvenlig, lavprisløsning til spildevandsrensningKredit:somsak nitimongkolchai, Shutterstock Forskere udviklede et bæredygtigt spildevandsbehandlingssystem lavet af landbrugs- og industriaffald. Ifølge FNs skøn, to tredjedele af verdens befolkn
En miljøvenlig, lavprisløsning til spildevandsrensningKredit:somsak nitimongkolchai, Shutterstock Forskere udviklede et bæredygtigt spildevandsbehandlingssystem lavet af landbrugs- og industriaffald. Ifølge FNs skøn, to tredjedele af verdens befolkn -
 Gennembrud for origami-diagnostik er til gavn for landmænd i udviklingslandeneKredit: ACS sensorer (2018). DOI:10.1021/acssensors.7b00825 Ark foldet papir, trykt med voks, kunne være nøglen til at udvikle meget billig diagnostik for at forbedre sundheden for husdyr i lav-
Gennembrud for origami-diagnostik er til gavn for landmænd i udviklingslandeneKredit: ACS sensorer (2018). DOI:10.1021/acssensors.7b00825 Ark foldet papir, trykt med voks, kunne være nøglen til at udvikle meget billig diagnostik for at forbedre sundheden for husdyr i lav- -
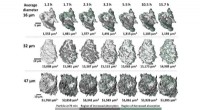 Cementerer fremtidenBilleddannelse af udviklingen af tre cementpartikler. Grøn indikerer opløste mineraler, hulrum og mineralske forbindelser med lav masse. Mørkegrå indikerer solide materialer. Billeddannelsen indiker
Cementerer fremtidenBilleddannelse af udviklingen af tre cementpartikler. Grøn indikerer opløste mineraler, hulrum og mineralske forbindelser med lav masse. Mørkegrå indikerer solide materialer. Billeddannelsen indiker
- Sammenlign vulkansk krater med en caldera?
- Ligning i reaktionerne fra benzylalkohol og natriummetal?
- Dræber Nil-krokodiller i Florida? Eksperter siger, at det er muligt
- To satellitter undgik lige et frontalt smadder:Hvor tæt kom de på en katastrofe?
- Udforskning af, hvordan overflader ændrer sig i kontakt med reaktive gasfaser under forskellige for…
- Forskning viser iskapper så store som Grønland smeltede hurtigt i et opvarmende klima


