Ionisk bindingsopløselighed i vand:En omfattende forklaring
* Polaritet: Vandmolekyler er polære, hvilket betyder, at de har en positiv ende (brint) og en negativ ende (ilt). Dette gør det muligt for vandmolekyler at omgive ioner og trække dem fra hinanden.
* Elektrostatiske interaktioner: Den positive ende af et vandmolekyle kan tiltrække den negative ion, mens den negative ende kan tiltrække den positive ion. Dette svækker den elektrostatiske tiltrækning mellem ionerne i den ioniske forbindelse, hvilket fører til opløsning.
Der er dog undtagelser:
* Gitterenergi: Nogle ioniske forbindelser har meget stærke elektrostatiske tiltrækninger (høj gitterenergi). Disse forbindelser opløses muligvis ikke let i vand. For eksempel er calciumcarbonat (CaCO3) kun lidt opløseligt i vand.
* Hydreringsenergi: Den energi, der frigives, når ioner er omgivet af vandmolekyler (hydreringsenergi), skal være tilstrækkelig til at overvinde gitterenergien, for at opløsning kan ske.
* Almindelig ioneffekt: Hvis opløsningen allerede indeholder en høj koncentration af en af ionerne fra den ioniske forbindelse, vil opløseligheden af forbindelsen blive reduceret.
Opsummering: De fleste ioniske forbindelser er opløselige i vand på grund af vands polære natur og de elektrostatiske interaktioner mellem vandmolekyler og ionerne. Imidlertid kan faktorer som gitterenergi, hydreringsenergi og den almindelige ioneffekt påvirke opløseligheden.
Sidste artikelSaltsyre og fordøjelse:Hvordan det nedbryder mad
Næste artikelForståelse af 'l' i kemi:kvantetal og mere
 Varme artikler
Varme artikler
-
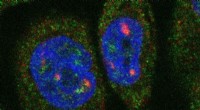 Design af lægemidler rettet mod en anden del af livets kodeIndividuelle RNA-molekyler fluorescerer inde i en brystkræftcelle. Kredit:Sunjong Kwon, Oregon Health &Science University, via Flickr De fleste lægemidler virker ved at pille ved proteiners adfærd
Design af lægemidler rettet mod en anden del af livets kodeIndividuelle RNA-molekyler fluorescerer inde i en brystkræftcelle. Kredit:Sunjong Kwon, Oregon Health &Science University, via Flickr De fleste lægemidler virker ved at pille ved proteiners adfærd -
 Opdagelse af overgangsmetalkatalysator kan hjælpe med at etablere vedvarende genereret elektricitetEt hold af KAUST-katalysatorforskere har vist, hvordan en molybdæn-baseret katalysator (billedet ovenfor) kan spille en central rolle i en proces, der er afgørende for bæredygtig produktion af vedvare
Opdagelse af overgangsmetalkatalysator kan hjælpe med at etablere vedvarende genereret elektricitetEt hold af KAUST-katalysatorforskere har vist, hvordan en molybdæn-baseret katalysator (billedet ovenfor) kan spille en central rolle i en proces, der er afgørende for bæredygtig produktion af vedvare -
 Nye kemiske mekanismer identificeret på vej til renere, mere effektiv forbrændingSandia National Laboratories-forsker Nils Hansen bruger en enhed kaldet en jet-omrørt reaktor til at udføre kemisk forskning, der tilføjer den grundlæggende viden om forbrænding. Kredit:Dino Vournas
Nye kemiske mekanismer identificeret på vej til renere, mere effektiv forbrændingSandia National Laboratories-forsker Nils Hansen bruger en enhed kaldet en jet-omrørt reaktor til at udføre kemisk forskning, der tilføjer den grundlæggende viden om forbrænding. Kredit:Dino Vournas -
 Med mere lys, kemien tager fartNogle kemiske reaktioner kan fremskyndes ved at øge intensiteten af belysning - dette er blevet demonstreret af forskere fra Institut for Fysisk Kemi ved det polske videnskabsakademi i Warszawa. Kre
Med mere lys, kemien tager fartNogle kemiske reaktioner kan fremskyndes ved at øge intensiteten af belysning - dette er blevet demonstreret af forskere fra Institut for Fysisk Kemi ved det polske videnskabsakademi i Warszawa. Kre
- Hvordan rejser en elektron gennem et kredsløb?
- Dinitrogenmonoxid (N₂O):Struktur, egenskaber og binding
- Astronomer afslører ny indsigt i oprindelsen og udviklingen af den åbne klynge NGC 6791
- Jeg ridser din, hvis du min:Hvordan rotter hjælper hinanden
- Hvad er den tid, det tager for Jorden at gøre en komplet bane omkring solen?
- Hvad er en tilstand af stof, der har fast form, men ikke volumen?


