Dinitrogenmonoxid (N₂O):Struktur, egenskaber og binding
Struktur:
* Centralt atom: Nitrogen (N)
* Terminale atomer: To oxygen (O) atomer
* Binding:
* Det centrale nitrogenatom er bundet til begge oxygenatomer gennem en dobbeltbinding og en enkeltbinding .
* Iltatomerne er forbundet gennem en koordinatkovalent binding , hvor et af iltatomerne donerer begge elektroner for at danne bindingen.
Lewis-struktur:
```
O
||
N - N
||
O
```
Egenskaber:
* Farveløs gas: Ved stuetemperatur er det en farveløs gas med en let sødlig lugt.
* Lidt opløseligt i vand: Det opløses i ringe grad i vand.
* Lattergas: Kendt for sine bedøvende og mildt euforiske virkninger, hvorfor det kaldes "lattergas".
* Oxidator: Det kan fungere som et oxidationsmiddel i visse reaktioner.
* Bruges i tandplejen: Dinitrogenoxid bruges som et mildt bedøvelsesmiddel ved tandbehandlinger.
* Anden anvendelse: Det bruges også som drivmiddel i flødeskumsdåser, som tilsætningsstof i raketbrændstof og i fødevareindustrien.
Kovalent binding:
Dinitrogenmonoxid er en kovalent forbindelse, fordi nitrogen- og oxygenatomerne deler elektroner for at danne bindinger. Denne deling af elektroner resulterer i et mere stabilt arrangement af atomer.
 Varme artikler
Varme artikler
-
 Forebyggelse af lithiumtab for højkapacitets lithium-ion-batterierKredit:Korea Institute of Science and Technology Et hold af koreanske forskere har udviklet en behandlingsteknologi til at maksimere energitætheden for batterier med høj kapacitet. Det fælles fors
Forebyggelse af lithiumtab for højkapacitets lithium-ion-batterierKredit:Korea Institute of Science and Technology Et hold af koreanske forskere har udviklet en behandlingsteknologi til at maksimere energitætheden for batterier med høj kapacitet. Det fælles fors -
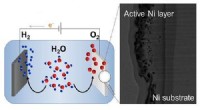 Opdeling af vand til prisen for et nikkelEt elektronmikroskopbillede af en nikkelanode (til højre), der øger ilt-udviklingsreaktionen, der er vigtig for vandspaltning (til venstre). Kredit:KAUST En teknik til at skabe et materiale til om
Opdeling af vand til prisen for et nikkelEt elektronmikroskopbillede af en nikkelanode (til højre), der øger ilt-udviklingsreaktionen, der er vigtig for vandspaltning (til venstre). Kredit:KAUST En teknik til at skabe et materiale til om -
 Ny sommerfugl-inspireret brintsensor drives af lysPh.d.-forsker Ebtsam Alenezy har en prototype af den lysaktiverede brintsensor, som kan levere ultrapræcise resultater ved stuetemperatur. Kredit:RMIT University Inspireret af overfladen af somm
Ny sommerfugl-inspireret brintsensor drives af lysPh.d.-forsker Ebtsam Alenezy har en prototype af den lysaktiverede brintsensor, som kan levere ultrapræcise resultater ved stuetemperatur. Kredit:RMIT University Inspireret af overfladen af somm -
 Bakteriefilm adskiller vand fra olieBakteriel cellulose viste nytte til at adskille olie og vand i eksperimenter ledet ved NC State. Kredit:Zahra Ashrafi Forskere har påvist, at en slimet, dog hård, type biofilm, som visse bakterier
Bakteriefilm adskiller vand fra olieBakteriel cellulose viste nytte til at adskille olie og vand i eksperimenter ledet ved NC State. Kredit:Zahra Ashrafi Forskere har påvist, at en slimet, dog hård, type biofilm, som visse bakterier
- Hvad er den kemiske formel for iodat?
- Hvilket element vil have en ædelgaskonfiguration, hvis det danner en ionisk binding ved at accepter…
- Hvad går lys baglæns, men tungt fremad?
- 2838 ml svarer til hvor mange liter?
- Virksomheder slører dårlige nyheder i finansielle rapporter, undersøgelse tyder på
- Hvad er 10 ting, der flyder?


