Metal renhed og stabilitet:Forstå forskellen mellem metaller og malme
* Oxidationstilstand: Malme er forbindelser, hvor metallet er i en kombineret tilstand, ofte med ilt eller andre grundstoffer. Det betyder, at metalatomet har mistet elektroner og eksisterer i en højere oxidationstilstand. Rene metaller har på den anden side en neutral oxidationstilstand.
* Reaktivitet: Metaller i malme er ofte mere reaktive på grund af deres højere oxidationstilstand. De er mere tilbøjelige til at gennemgå yderligere reaktioner og transformationer. Rene metaller er mindre reaktive og mere stabile.
* Energitilstand: Det kræver energi at udvinde metallet fra dets malm, bryde bindingerne og reducere metallet til dets elementære tilstand. Dette tyder på, at det rene metal er i en lavere energitilstand og derfor mere stabilt.
Eksempel: Jernmalm (Fe2O3) er mindre stabil end rent jern (Fe). Jernet i malmen oxideres, mens det rene jern er i sin elementære form. For at opnå rent jern skal vi reducere jernoxidet i en højtemperaturproces, som kræver energi.
Undtagelser:
* Ædelmetaller: Nogle metaller, som guld og platin, findes naturligt i deres rene form. De er i sagens natur mindre reaktive og allerede i deres mest stabile form.
* Legeringer: Nogle legeringer, blandinger af forskellige metaller, kan være mere stabile end deres individuelle komponenter. Kombinationen af metaller kan skabe en mere modstandsdygtig struktur.
Som konklusion: Selvom der er undtagelser, er rene metaller generelt mere stabile end deres malme på grund af deres lavere oxidationstilstand, reducerede reaktivitet og lavere energitilstand.
Sidste artikelSmeltning:Udvinding af metaller fra malme - En omfattende guide
Næste artikelMetals from Ore:A Guide to Extraction Processes
 Varme artikler
Varme artikler
-
 Indbygget gassensorenhed lover enkel, nøjagtig påvisning af flygtige organiske forbindelserI gennemgang af videnskabelige instrumenter, forskere ved Gdańsk University of Technology beskriver en måleanordning designet til at analysere luftprøver indeholdende forskellige flygtige organiske fo
Indbygget gassensorenhed lover enkel, nøjagtig påvisning af flygtige organiske forbindelserI gennemgang af videnskabelige instrumenter, forskere ved Gdańsk University of Technology beskriver en måleanordning designet til at analysere luftprøver indeholdende forskellige flygtige organiske fo -
 Brug af bakterier fra varme kilder, biokemiker studerer RNA-splejsning hos menneskerAaron Robart, Assisterende professor, WVU School of Medicine, Institut for Biokemi. Kredit:Aira Burkhart/West Virginia University Omkring 70 procent af det menneskelige genom koder ikke for noget.
Brug af bakterier fra varme kilder, biokemiker studerer RNA-splejsning hos menneskerAaron Robart, Assisterende professor, WVU School of Medicine, Institut for Biokemi. Kredit:Aira Burkhart/West Virginia University Omkring 70 procent af det menneskelige genom koder ikke for noget. -
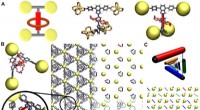 Fysikere afkoder den dynamiske interaktion mellem molekylære maskiner i metal-organiske rammerMolekylær struktur af den rotaxanfunktionaliserede MOF.(A ) Repræsentation af én organisk linker, der forbinder fire uorganiske Zn4 O hjørner. Det venstre billede skitserer byggestenens struktur, det
Fysikere afkoder den dynamiske interaktion mellem molekylære maskiner i metal-organiske rammerMolekylær struktur af den rotaxanfunktionaliserede MOF.(A ) Repræsentation af én organisk linker, der forbinder fire uorganiske Zn4 O hjørner. Det venstre billede skitserer byggestenens struktur, det -
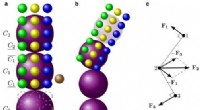 Computermodeller giver ny forståelse af seglcellesygdomEn ny modelleringsteknik gør det muligt for forskere at se, hvad der sker inde i røde blodlegemer, der er ramt af seglcellesygdom. Kredit:Karniadakis lab / Brown University Computermodeller udvikl
Computermodeller giver ny forståelse af seglcellesygdomEn ny modelleringsteknik gør det muligt for forskere at se, hvad der sker inde i røde blodlegemer, der er ramt af seglcellesygdom. Kredit:Karniadakis lab / Brown University Computermodeller udvikl


