Forståelse af surheden af grundvand:Kulsyrens rolle
* CO2 Absorption: Når regnvand siver gennem jorden og klipperne, opløser det atmosfærisk CO2, som er en naturlig bestanddel af luften.
* Kulsyredannelse: Opløst CO2 reagerer med vand og danner kulsyre (H2CO3):
CO2 + H2O ⇌ H2CO3
* Svag syre: Kulsyre er en svag syre, hvilket betyder, at den kun delvist ioniserer i vand og frigiver hydrogenioner (H+) og bicarbonationer (HCO3-):
H2CO3 ⇌ H+ + HCO3-
* pH-niveau: Tilstedeværelsen af disse hydrogenioner gør underjordisk vand let surt, typisk med et pH-område på 6,5 til 7,5.
Faktorer, der påvirker surhedsgraden:
* CO2-niveauer: Mængden af CO2 opløst i vand afhænger af partialtrykket af CO2 i atmosfæren og mængden af kontakt mellem vand og luft.
* Rocktype: Typerne af sten og mineraler under jorden kan påvirke vandets surhedsgrad. Nogle sten, som kalksten, kan buffer surhedsgraden ved at reagere med kulsyre.
* Temperatur: Højere temperaturer fører generelt til lavere CO2-opløselighed, hvilket kan mindske surhedsgraden.
Betydning af pH:
pH-værdien af underjordisk vand er vigtig, fordi den påvirker:
* Mineralopløsning: Surt vand kan opløse mineraler i de omkringliggende bjergarter, som kan påvirke vandets kemiske sammensætning.
* Biologiske processer: pH-værdien påvirker overlevelsen og aktiviteten af organismer, der lever i vandet.
* Korrosion: Surt vand kan korrodere rør og anden infrastruktur.
Opsummering: Selvom det ikke altid er stærkt surt, er underjordisk vand ofte let surt på grund af tilstedeværelsen af opløst kuldioxid, som danner kulsyre. Surhedsgraden kan variere afhængigt af forskellige faktorer.
 Varme artikler
Varme artikler
-
 Videnskab ved grænsefladen:Bioinspirerede materialer afslører nyttige egenskaberNy forskning af Brian Wadsworth, Gary Moore og deres kolleger pryder forsiden af tidsskriftet ACS Materials &Interfaces. Inspireret af naturen, hvor aminosyrerester og bløde materialers koordination
Videnskab ved grænsefladen:Bioinspirerede materialer afslører nyttige egenskaberNy forskning af Brian Wadsworth, Gary Moore og deres kolleger pryder forsiden af tidsskriftet ACS Materials &Interfaces. Inspireret af naturen, hvor aminosyrerester og bløde materialers koordination -
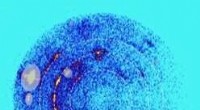 Meteoritnedslag kan skabe uventede former for silicaRøntgendiffraktionsbilleder, der viser den nye form for silica skabt ved at sende en intens stødbølge gennem en prøve af kvarts ved hjælp af en specialiseret gaspistol. Når røntgenstrålerne preller af
Meteoritnedslag kan skabe uventede former for silicaRøntgendiffraktionsbilleder, der viser den nye form for silica skabt ved at sende en intens stødbølge gennem en prøve af kvarts ved hjælp af en specialiseret gaspistol. Når røntgenstrålerne preller af -
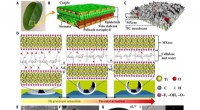 Bioinspireret MXene-baserede aktuatorer til programmerbare smartenhederDen udførlige struktur, komponenter, og aktiveringsmekanisme for den MXene-cellulosebaserede aktuator. (A) Fotografi af et naturligt blad. (B) Skematisk diagram af en bladstruktur. (C) Skematisk diagr
Bioinspireret MXene-baserede aktuatorer til programmerbare smartenhederDen udførlige struktur, komponenter, og aktiveringsmekanisme for den MXene-cellulosebaserede aktuator. (A) Fotografi af et naturligt blad. (B) Skematisk diagram af en bladstruktur. (C) Skematisk diagr -
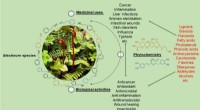 Forskere gennemgår anvendelser, fytokemi og farmakologiske egenskaber af slægten BlechnumMedicinsk anvendte Blechnum-planter. Kredit:WBG Flere værdifulde bregner, der tilhører slægten Blechnum, driver fra gård til traditionel helbredelse og etnofarmakologi, og er potentielle midler til
Forskere gennemgår anvendelser, fytokemi og farmakologiske egenskaber af slægten BlechnumMedicinsk anvendte Blechnum-planter. Kredit:WBG Flere værdifulde bregner, der tilhører slægten Blechnum, driver fra gård til traditionel helbredelse og etnofarmakologi, og er potentielle midler til


