Beregning af teoretisk udbytte af aluminiumoxid:en trin-for-trin guide
1. Skriv den afbalancerede kemiske ligning:
4 Al + 3 O2 -> 2 A1203
2. Bestem den begrænsende reaktant:
* Moler Al: 3,40 mol
* Moler O₂: 2,85 mol
For at finde den begrænsende reaktant skal vi sammenligne molforholdene baseret på den afbalancerede ligning:
* For Al: (3,40 mol Al) / (4 mol Al fra ligning) =0,85
* For O₂: (2,85 mol O2) / (3 mol O2 fra ligning) =0,95
Den mindre værdi (0,85) svarer til aluminium. Derfor er aluminium den begrænsende reaktant .
3. Beregn det teoretiske udbytte af Al₂O₃:
Da aluminium er den begrænsende reaktant, bruger vi dens mol til at beregne det teoretiske udbytte af aluminiumoxid:
* Fra den balancerede ligning: 4 mol Al producerer 2 mol Al203
* Forhold: (2 mol A1203)/(4 mol Al) =0,5 mol A1203/mol Al
* Teoretisk udbytte: (3,40 mol Al) * (0,5 mol Al2O3/mol Al) =1,70 mol Al2O3
Derfor er det teoretiske udbytte af aluminiumoxid 1,70 mol.
Bemærk: For at konvertere mol til gram, skal du bruge den molære masse af aluminiumoxid (101,96 g/mol).
Sidste artikelForklaret pH-skala:Forståelse af surhedsgrad og hydrogenioner
Næste artikelForståelse af surheden af grundvand:Kulsyrens rolle
 Varme artikler
Varme artikler
-
 AI-agent hjælper med at identificere materialeegenskaber hurtigereKredit:CC0 Public Domain Effektiv analyse af røntgendiffraktionsdata (XRD) spiller en afgørende rolle i opdagelsen af nye materialer, for eksempel for fremtidens energisystemer. Det bruges til a
AI-agent hjælper med at identificere materialeegenskaber hurtigereKredit:CC0 Public Domain Effektiv analyse af røntgendiffraktionsdata (XRD) spiller en afgørende rolle i opdagelsen af nye materialer, for eksempel for fremtidens energisystemer. Det bruges til a -
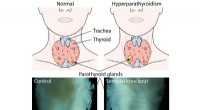 Opdagelse af signalprotein kan føre til lægemiddelbaserede terapier til behandling af hyperparathy…Fire små biskjoldbruskkirtler placeret i nakken bag den større skjoldbruskkirtel er ansvarlige for at styre sunde blodcalciumniveauer. Primær hyperparatyreoidisme er præget af overdreven parathyreoide
Opdagelse af signalprotein kan føre til lægemiddelbaserede terapier til behandling af hyperparathy…Fire små biskjoldbruskkirtler placeret i nakken bag den større skjoldbruskkirtel er ansvarlige for at styre sunde blodcalciumniveauer. Primær hyperparatyreoidisme er præget af overdreven parathyreoide -
 Forskere finder en miljøvenlig måde at farve blå jeans påProcessen med at farve jeans er en af de største kilder til forurening inden for modeindustrien. Ny forskning fandt et mere miljøvenligt alternativ. Kredit:Andrew Davis Tucker/UGA Blusset eller
Forskere finder en miljøvenlig måde at farve blå jeans påProcessen med at farve jeans er en af de største kilder til forurening inden for modeindustrien. Ny forskning fandt et mere miljøvenligt alternativ. Kredit:Andrew Davis Tucker/UGA Blusset eller -
 Hurtig, fleksibel vandanalyse skaber røre i industrienKredit:CYTO-WATER Det EU-finansierede CYTO-WATER-projekt har udviklet et innovativt analysesystem på stedet, der er i stand til hurtigt at detektere forskellige mikroorganismer i vand. Den analyt
Hurtig, fleksibel vandanalyse skaber røre i industrienKredit:CYTO-WATER Det EU-finansierede CYTO-WATER-projekt har udviklet et innovativt analysesystem på stedet, der er i stand til hurtigt at detektere forskellige mikroorganismer i vand. Den analyt
- Hvad er formålet?
- Iagttagelse og eksperimentering er to måder, hvorpå økologer kan besvare videnskabelige spørgsmå…
- Omfattende kig på det grundlæggende i de mest ønskværdige nanorør
- Dødstallet for oversvømmelser i Japan stiger til 30
- Havliv fundet i oldtidens Antarktis is hjælper med at løse et kuldioxidpuslespil fra istiden
- Nærmer sig videnskabsdata på en subjektiv måde?


