Svag syre + stærk basereaktion:en detaljeret forklaring
1. Dissociation:
* Stærk base: En stærk base som NaOH dissocierer fuldstændigt i vand og frigiver hydroxidioner (OH-) i opløsningen.
* Svag syre: En svag syre som eddikesyre (CH3COOH) dissocierer kun delvist i vand og frigiver en lille mængde hydrogenioner (H+) og dens konjugerede base (CH3COO-).
2. Neutralisering:
* Hydroxidionerne (OH-) fra den stærke base reagerer med hydrogenionerne (H+) fra den svage syre og danner vand (H2O).
* Denne reaktion forbruger H+ ionerne og flytter ligevægten af den svage syres dissociation til højre, hvilket får mere af den svage syre til at dissociere.
3. Saltdannelse:
* Den resterende konjugerede base af den svage syre (CH3COO-) kombineres med metalkationen fra den stærke base (Na+) og danner et salt (natriumacetat, CH3COONa).
4. pH-ændring:
* Reaktionen flytter opløsningens pH mod neutralitet. Da den stærke base er i overskud, vil den resulterende opløsning være let basisk (pH større end 7).
Nøglefunktioner:
* Bufferdannelse: Hvis den svage syre og dens konjugatbase er til stede i betydelige mængder, kan den resulterende opløsning fungere som en buffer, der modstår ændringer i pH.
* Ufuldstændig neutralisering: I modsætning til reaktionen mellem en stærk syre og en stærk base, er neutraliseringen af en svag syre med en stærk base ikke fuldstændig. Noget af den svage syre forbliver udissocieret, hvilket fører til en let basisk opløsning.
Eksempel:
Overvej reaktionen af eddikesyre (CH3COOH) med natriumhydroxid (NaOH):
CH3COOH(aq) + NaOH(aq) -> CH3COONa(aq) + H2O(l)
Denne reaktion producerer natriumacetat (CH3COONa), som er et salt, og vand. Opløsningen vil have en pH lidt større end 7 på grund af tilstedeværelsen af konjugatbasen af den svage syre.
Opsummering:
Reaktionen af en svag syre og en stærk base resulterer i neutralisering, saltdannelse og en let basisk opløsning. Den resulterende opløsning kan også fungere som en buffer afhængigt af de relative koncentrationer af den svage syre og dens konjugatbase.
 Varme artikler
Varme artikler
-
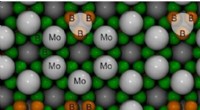 Forskere beregner krystalstruktur af superhårde molybdænboriderAtomarrangement i den højeste molybdænborid (MoB5-x) krystal Kredit:Dmitry V. Rybkovskiy, J. Phys. Chem. Lett. I deres søgen efter nye superhårde forbindelser, forskere har udført en forudsigelse
Forskere beregner krystalstruktur af superhårde molybdænboriderAtomarrangement i den højeste molybdænborid (MoB5-x) krystal Kredit:Dmitry V. Rybkovskiy, J. Phys. Chem. Lett. I deres søgen efter nye superhårde forbindelser, forskere har udført en forudsigelse -
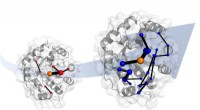 Forståelse af enzymudvikling baner vejen for grøn kemiLaboratorieudvikling af et designerenzym gør det til en meget bedre katalysator. Simuleringer viser, at evolutionen gør dette ved at indføre netværk af aminosyrer. Disse netværk lover at være skabelon
Forståelse af enzymudvikling baner vejen for grøn kemiLaboratorieudvikling af et designerenzym gør det til en meget bedre katalysator. Simuleringer viser, at evolutionen gør dette ved at indføre netværk af aminosyrer. Disse netværk lover at være skabelon -
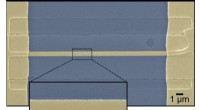 Grænser ingen barriere for termoelektricitetEt scanningselektronmikroskopbillede viser en nanotråd af en krystalguld på et termisk oxid-substrat. Forskere fra Rice University viste, at belastning og defekter i materialet kan ændre dets termoele
Grænser ingen barriere for termoelektricitetEt scanningselektronmikroskopbillede viser en nanotråd af en krystalguld på et termisk oxid-substrat. Forskere fra Rice University viste, at belastning og defekter i materialet kan ændre dets termoele -
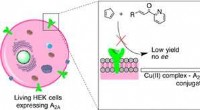 Kunstige enzymer udfører reaktioner på levende cellerKredit:American Chemical Society Naturen har udviklet tusindvis af enzymer for at lette de mange kemiske reaktioner, der finder sted inde i organismer for at opretholde liv. Nu, forskere har desig
Kunstige enzymer udfører reaktioner på levende cellerKredit:American Chemical Society Naturen har udviklet tusindvis af enzymer for at lette de mange kemiske reaktioner, der finder sted inde i organismer for at opretholde liv. Nu, forskere har desig
- Forstå årsagerne til truede levesteder
- Hvorfor er gravitation Bewteen små genstande ikke observeret?
- Reduktion af naturbrandrisici for bedre styring og ressourceallokering
- Hvordan produceres absorptions- og emissionslinjer i et fantastisk spektrum Hvilke oplysninger kan s…
- Karakteristik af en dværgplanet
- Lithium Det første element i gruppe 1 har et atomnummer på 3 sekund dette atomiknumre Hvad?


