Forståelse af hydroxylioner (OH⁻):egenskaber og rolle i baser
* En negativ ladning: Hydroxylioner har en enkelt negativ ladning (OH⁻). Dette skyldes, at de dannes, når et vandmolekyle mister en proton (H⁺).
* Et oxygenatom bundet til et hydrogenatom: Hydroxylionen består af et oxygenatom (O) kovalent bundet til et hydrogenatom (H).
* Evnen til at acceptere en proton: Hydroxylioner er basiske, fordi de kan acceptere en proton (H⁺) for at danne vand (H2O). Dette er nøgleegenskaben ved en base - den kan neutralisere en syre ved at acceptere dens proton.
Sammenfattende er en hydroxylion (OH⁻) et negativt ladet molekyle med et oxygenatom bundet til et hydrogenatom. Den er ansvarlig for en løsnings grundlæggende egenskaber.
 Varme artikler
Varme artikler
-
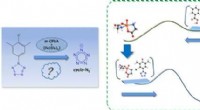 Forskere optrævler syntetisk mekanisme for arylpentazol og substituenteffekthttps://doi.org/10.1021/acs.jpclett.9b03762 Copyright © 2020 American Chemical Society For nylig, et forskerhold ledet af prof. Liu Jianyong og prof. Han Keli fra Dalian Institute of Chemical Phys
Forskere optrævler syntetisk mekanisme for arylpentazol og substituenteffekthttps://doi.org/10.1021/acs.jpclett.9b03762 Copyright © 2020 American Chemical Society For nylig, et forskerhold ledet af prof. Liu Jianyong og prof. Han Keli fra Dalian Institute of Chemical Phys -
 Nøglen til kulfrie biler? Se til stjernerneIllustration af en supernovaeksplosion. Sådanne hvirvlende masser af stof gav form til de tidligste former for kulstof - forstadier til molekyler, som nogle forskere siger, er forbundet med syntesen a
Nøglen til kulfrie biler? Se til stjernerneIllustration af en supernovaeksplosion. Sådanne hvirvlende masser af stof gav form til de tidligste former for kulstof - forstadier til molekyler, som nogle forskere siger, er forbundet med syntesen a -
 Svovlindhold i nogle højtydende stoffer svækker dem, når de udsættes for fugtPh.d.-studerende Saiful Hoque ledede ny forskning, der kunne vise vejen til at udvikle stærkere, sikrere beskyttelsestøj til brandmænd og andre arbejdere. Kredit:University of Alberta Forskere har
Svovlindhold i nogle højtydende stoffer svækker dem, når de udsættes for fugtPh.d.-studerende Saiful Hoque ledede ny forskning, der kunne vise vejen til at udvikle stærkere, sikrere beskyttelsestøj til brandmænd og andre arbejdere. Kredit:University of Alberta Forskere har -
 3-D-print af grønnere bygninger ved hjælp af lokal jordForskere har udviklet en metode til at 3D-printe strukturer ved hjælp af lokal jord. Kredit:Aayushi Bajpayee Byggebranchen står i øjeblikket over for to store udfordringer:efterspørgslen efter bær
3-D-print af grønnere bygninger ved hjælp af lokal jordForskere har udviklet en metode til at 3D-printe strukturer ved hjælp af lokal jord. Kredit:Aayushi Bajpayee Byggebranchen står i øjeblikket over for to store udfordringer:efterspørgslen efter bær
- Forbindelsens molekylære masse er 132 amu Hvilken formel?
- Virtuel skolegang afslører digitale udfordringer for sorte familier, undersøgelse finder
- Hvad er de motoriske dele af kroppen?
- Gør produkter mere biologisk nedbrydelige med stivelse
- Hvor er den kinetiske energi maksimalt?
- Hvad bestemmer en form?


