Molekylær geometri af NH3 (ammoniak):En detaljeret forklaring
Her er hvorfor:
* Centralt atom: Nitrogen (N)
* Antal valenselektroner: Nitrogen har 5 valenselektroner.
* Antal bindingspar: Nitrogen danner 3 enkeltbindinger med 3 hydrogenatomer (H).
* Antal enlige par: Nitrogen har ét ensomt elektronpar.
VSEPR-teori: Valence Shell Electron Pair Repulsion teorien forudsiger, at elektronpar omkring et centralt atom vil arrangere sig selv for at minimere frastødning. Dette fører til følgende:
* De 3 bindingspar og 1 enlige par omkring nitrogenatomet vil arrangere sig selv i en tetraedrisk form.
* Det enlige par optager dog mere plads end bindingsparrene, hvilket presser brintatomerne tættere på hinanden.
* Dette resulterer i en forvrænget tetraedrisk form, specifikt en trigonal pyramideformet geometri.
Visuel repræsentation: Forestil dig en pyramide med et nitrogenatom i spidsen og de tre hydrogenatomer i bunden. Det enlige par på nitrogenet er placeret over bunden af pyramiden.
 Varme artikler
Varme artikler
-
 Hvad driver hydrogenbinding?Hydrogenbinding er en hjørnesten i kemi, der understøtter adfærden af utallige stoffer - især vand. At forstå, hvorfor disse bindinger dannes, er afgørende for en dybere forståelse af intermolekylære
Hvad driver hydrogenbinding?Hydrogenbinding er en hjørnesten i kemi, der understøtter adfærden af utallige stoffer - især vand. At forstå, hvorfor disse bindinger dannes, er afgørende for en dybere forståelse af intermolekylære -
 Ny modelleringstilgang hjælper laserglasdesignMålte og kurvetilpasning afledte IR-spektre af P, PL, PN glasprøver, og individuelle bånd af P-glas ifølge litteratur. Kredit:SIOM Nd-doterede fosfatglas bruges i laserapplikationer med høj energi
Ny modelleringstilgang hjælper laserglasdesignMålte og kurvetilpasning afledte IR-spektre af P, PL, PN glasprøver, og individuelle bånd af P-glas ifølge litteratur. Kredit:SIOM Nd-doterede fosfatglas bruges i laserapplikationer med høj energi -
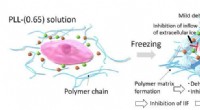 Ny indsigt sætter en stopper for mekanismerne til sikker kryokonservering af biologiske materialerNår celler fryses med PLL-(0,65), fryseprocessen koncentrerer PLL-(0,65)-molekylerne, hvilket igen får dem til at aggregeres på grund af stærke intermolekylære attraktionskræfter. Denne aggregering af
Ny indsigt sætter en stopper for mekanismerne til sikker kryokonservering af biologiske materialerNår celler fryses med PLL-(0,65), fryseprocessen koncentrerer PLL-(0,65)-molekylerne, hvilket igen får dem til at aggregeres på grund af stærke intermolekylære attraktionskræfter. Denne aggregering af -
 Superkritisk svar på spildolie fundetKredit:Pixabay/CC0 Public Domain Smøreolier nedbrydes og oxiderer ved brug samt akkumulerer partikler fra de motorer og andre maskiner, hvori de bruges. Ultimativt, deres effektivitet forværres, o
Superkritisk svar på spildolie fundetKredit:Pixabay/CC0 Public Domain Smøreolier nedbrydes og oxiderer ved brug samt akkumulerer partikler fra de motorer og andre maskiner, hvori de bruges. Ultimativt, deres effektivitet forværres, o
- Hvorfor har astronauter mindre vægt på månen end på jorden?
- Utroligt:Astronomer hylder de første billeder af asteroide-nedslag
- Klimaændringer får buske og træer til at udvide sig nordpå i subarktis
- Stealth-nanopartikler kunne forbedre kræftvacciner
- Hvilken energioverførsel bevæger varme plader i jorden?
- Metoden til at gruppere organismer i kategorier, der repræsenterer linjer Evolutionær afstamning k…


