Ny indsigt sætter en stopper for mekanismerne til sikker kryokonservering af biologiske materialer
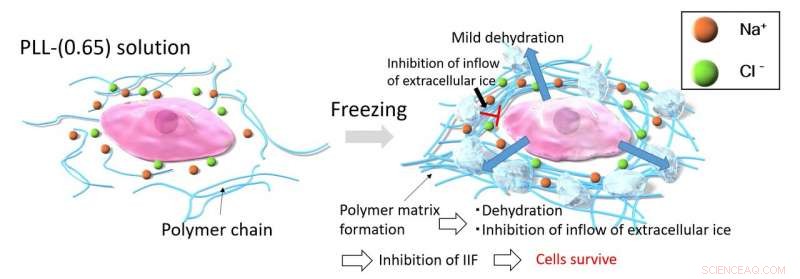
Når celler fryses med PLL-(0,65), fryseprocessen koncentrerer PLL-(0,65)-molekylerne, hvilket igen får dem til at aggregeres på grund af stærke intermolekylære attraktionskræfter. Denne aggregering af PLL-(0,65) fanger ioner og vand i matrixen for at forhindre enhver dramatisk osmotisk ændring. Den tykke polymermatrix hæmmer tilstrømningen af ekstracellulær is ind i cellerne, som undgår problemet med intracellulær isdannelse (IIF). Billede:Kazuaki Matsumura fra JAIST.
Kryokonservering involverer konservering af biologiske materialer, såsom celler, væv, og organer, ved ultralave temperaturer, så de kan genoplives og bruges på et senere tidspunkt. For at opnå kryokonservering, så de konserverede materialer ikke beskadiges, forskere bruger forskellige kemikalier kaldet kryobeskyttelsesmidler, som letter nedfrysningsprocessen. Desværre, mange af de eksisterende kryobeskyttende midler har store begrænsninger. For eksempel, dimethylsulfoxid er nyttigt til kryokonservering af røde blodlegemer, men det er også giftigt for cellerne.
For at overvinde disse begrænsninger, forskere ved Japan Advanced Institute of Science and Technology (JAIST) og Japans RIKEN har eksperimenteret med en klasse af kemikalier kendt som polyamfolytter, identificere en polyamfolyt ved navn carboxyleret ε-poly-ʟ-lysin (COOH-PLL) som et lovende kryobeskyttelsesmiddel, der ikke har toksiske virkninger på celler.
Imidlertid, den mekanisme, hvormed COOH-PLL fungerer som et kryobeskyttelsesmiddel, forblev dårligt forstået, og dette hindrede bestræbelserne på at udvikle bedre polyamfolyt kryobeskyttelsesmidler. For at afhjælpe denne videnskløft, dette team af forskere, som blev ledet af professor Kazuaki Matsumura fra JAIST - og som også omfattede Asst. Prof. Robin Rajan fra JAIST og Dr. Fumiaki Hayashi og Dr. Toshio Nagashima fra RIKEN – udførte en anden undersøgelse, hvor de brugte en metode kaldet solid-state nuclear magnetic resonance (NMR) spektroskopi til at karakterisere, hvad der sker med vandmolekyler, natrium- og chloridioner, og en form for COOH-PLL kaldet PLL-(0,65), når de blandes og fryses til temperaturer, der bruges til kryokonservering. Deres resultater fremgår af en nylig udgave af det fagfællebedømte tidsskrift Communications Materials.
Som forventet, NMR-signalerne registreret fra disse frosne opløsninger indikerede reduceret mobilitet på molekylært niveau og øget opløsningsviskositet (dvs. øget modstand mod strømning) ved ultralave temperaturer. Vigtigt, PLL- (0,65) molekylerne fangede vandmolekylerne og ionerne på måder, der forhindrede dannelsen af intracellulære iskrystaller og modvirkede virkningerne af osmotisk chok (en form for fysiologisk dysfunktion, hvor en pludselig ændring i ionkoncentrationer omkring en celle kan føre til hurtig indstrømning eller udstrømning af væske til eller fra cellen beskadige det). Intracellulære iskrystaller og osmotisk shock er væsentlige årsager til cellulær eller vævsskade under frysning, så PLL-(0,65)'s evne til at forhindre begge er med til at forklare dets effektivitet som et kryobeskyttelsesmiddel.
Ved at beskrive den videnskabelige værdi af disse fund, Prof. Matsumura bemærker, at brugen af NMR "muliggjorde karakterisering af de kryoprotektive egenskaber af polymerer, der fungerer gennem andre mekanismer end de nuværende kryoprotektanter." Han forudser, at denne karakterisering "vil lette det molekylære design af nye kryobeskyttelsesmidler, " som vil "fremme den kliniske brug af polymere kryobeskyttende midler, der kan tjene som effektive alternativer til små molekylemidler såsom dimethylsulfoxid og glycerol."
Små molekyle kryobeskyttelsesmidler er kun nyttige til at bevare celler og små væv, men polymere kryobeskyttelsesmidler kan gøre det muligt for forskere at opnå kryokonservering af større vævsvolumener eller endda hele organer. Dette ville være et vigtigt fremskridt for nye områder som regenerativ medicin, som har til formål at genoprette normale fysiologiske funktioner ved at erstatte eller regenerere celler, væv, og organer.
Holdets resultater kan også have vigtige konsekvenser for grundlæggende biologi. I de seneste år, forskere har erfaret, at iboende forstyrrede proteiner, som mangler en fast tredimensionel form, tjene en vigtig rolle i beskyttelsen af celler mod skader i forbindelse med udtørring og osmotisk chok ved lave temperaturer. Fordi proteiner i sig selv er en klasse af polyampholytter, disse nyligt offentliggjorte resultater vedrørende COOH-PLL's adfærd ved ultralave temperaturer kan være med til at forklare de mekanismer, hvormed iboende forstyrrede proteiner beskytter celler. Yderligere forskning i mekanismerne af sådanne proteiner kan igen føre til udvikling af avancerede materialer med anvendelse i regenerativ medicin.
Afslutningsvis, disse fund kan have stor værdi for biologi og medicin. "Baseret på vores nu forbedrede forståelse af mekanismer af polymere kryobeskyttende midler, " bemærker prof. Matsumura, "Vi forventer at udvikle nye kryokonserveringsteknologier til store vævsvolumener og organer, som vil tillade implementering af regenerativ medicin i industriel skala via etablering af banker af konstrueret væv." Disse skridt hen imod regenerativ medicin vil gøre meget for at forbedre livet for mennesker, der lever med medicinske lidelser, der i øjeblikket er uhelbredelige.
 Varme artikler
Varme artikler
-
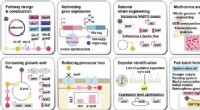 Konstrueret C. glutamicum stamme i stand til at producere glutarsyre på højt niveau fra glucoseSystemets metaboliske ingeniørstrategier anvendt til konstruktionen af en konstrueret C. glutamicum-stamme, der er i stand til effektivt at producere glutarsyre. Kredit:Korea Advanced Institute of S
Konstrueret C. glutamicum stamme i stand til at producere glutarsyre på højt niveau fra glucoseSystemets metaboliske ingeniørstrategier anvendt til konstruktionen af en konstrueret C. glutamicum-stamme, der er i stand til effektivt at producere glutarsyre. Kredit:Korea Advanced Institute of S -
 Søger uorden som en katalysator for forandringDr. Rosalie Hocking skinner lys på uordnede mineraler for at finde katalysatorer, der kan gøre vand til rent brændstof. Kredit:Swinburne University of Technology Grønne kemikere drømmer om at repl
Søger uorden som en katalysator for forandringDr. Rosalie Hocking skinner lys på uordnede mineraler for at finde katalysatorer, der kan gøre vand til rent brændstof. Kredit:Swinburne University of Technology Grønne kemikere drømmer om at repl -
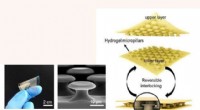 Forskere udvikler en ny klasse af undervandslimFotografi af det fremstillede fleksible sammenklæbende klæbemiddel (til venstre) og et SEM -billede (i midten) af PEGDMA mikrokrogarrays af klæbemidlet. Til højre er den konceptuelle illustration af d
Forskere udvikler en ny klasse af undervandslimFotografi af det fremstillede fleksible sammenklæbende klæbemiddel (til venstre) og et SEM -billede (i midten) af PEGDMA mikrokrogarrays af klæbemidlet. Til højre er den konceptuelle illustration af d -
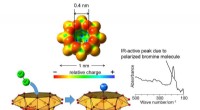 Polarisering af brommolekyle i vanadiumoxidklyngehulrum og ny alkanbromeringSpektrets top på grund af polariseret brommolekyle. Kredit:Kanazawa University Alkaner er hovedbestanddelene i naturgas og olie, kun bestående af kulstof- og brintatomer. CH-bindingerne af alkaner
Polarisering af brommolekyle i vanadiumoxidklyngehulrum og ny alkanbromeringSpektrets top på grund af polariseret brommolekyle. Kredit:Kanazawa University Alkaner er hovedbestanddelene i naturgas og olie, kun bestående af kulstof- og brintatomer. CH-bindingerne af alkaner
- Apps er blevet sikrere efter EU's generelle databeskyttelsesforordning
- Ingeniører gør kritiske fremskridt inden for kvantecomputerdesign
- En 3D multifunktionel og fleksibel neural grænseflade
- Klima forklaret:Hvordan hvide tage hjælper med at reflektere solens varme
- Magnetisme tænder og slukker frigivelse af lægemidler
- Limber mini-gepardrobot leverer en imponerende backflip-ydelse


