Hvad driver hydrogenbinding?
Hydrogenbinding er en hjørnesten i kemi, der understøtter adfærden af utallige stoffer - især vand. At forstå, hvorfor disse bindinger dannes, er afgørende for en dybere forståelse af intermolekylære kræfter og kemisk adfærd.
TL;DR
Hydrogenbinding opstår, når elektronegative atomer (O, N, F) trækker delte elektroner væk fra brint og skaber permanente dipoler, der tiltrækker hinanden på tværs af molekyler.
Elektronegativitet og permanente dipolmomenter
Når to atomer deler elektroner, afhænger fordelingen af elektrontæthed af deres elektronegativitet. Identiske elektronegativiteter giver en lige stor andel, men når et atom er mere elektronegativt, klynger de delte elektroner tættere på det. Denne ubalance giver det mere elektronegative atom en let negativ ladning og det mindre elektronegative atom en let positiv ladning, hvilket resulterer i et permanent dipolmoment - et polært molekyle.
Sådan dannes hydrogenbindinger
Polære molekyler har både en positivt ladet brintside og en negativt ladet heteroatomside. Når et molekyles brint nærmer sig det elektronegative atom i et andet, opstår der en attraktiv, intermolekylær interaktion - hydrogenbinding. Selvom de er svagere end kovalente bindinger (ca. en tiendedel af styrken), er disse bindinger afgørende for at bestemme de fysiske egenskaber af væsker og faste stoffer.
Brintbinding i vand
Vand (H2 O) eksemplificerer hydrogenbinding smukt. Oxygens højere elektronegativitet trækker elektrontætheden mod sig selv og efterlader brintatomer delvist positive. Hvert vandmolekyle kan donere to hydrogenbindinger (via dets to H-atomer) og acceptere to (via dets to enlige par på ilt). Dette omfattende netværk hæver vands kogepunkt over kogepunktet for lignende molekyler som ammoniak og forklarer isens lavere tæthed på grund af et åbent, hydrogenbundet gitter.
 Varme artikler
Varme artikler
-
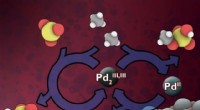 En ny måde at udnytte spildt metan påMIT kemiprofessor Yogesh Surendranath og tre kolleger har fundet en måde at bruge elektricitet på, som potentielt kan komme fra vedvarende kilder, at omdanne metan til derivater af methanol. Forskerne
En ny måde at udnytte spildt metan påMIT kemiprofessor Yogesh Surendranath og tre kolleger har fundet en måde at bruge elektricitet på, som potentielt kan komme fra vedvarende kilder, at omdanne metan til derivater af methanol. Forskerne -
 Forskere bruger grønt guld til hurtigt at opdage og identificere skadelige bakterierProfessor Abdennour Abbas og hans forskerhold har udført grundforskning i samspillet mellem guldnanopartikler og celleoverflader for at skabe nye sensorer. Forskelligt formede guldnanopartikler som de
Forskere bruger grønt guld til hurtigt at opdage og identificere skadelige bakterierProfessor Abdennour Abbas og hans forskerhold har udført grundforskning i samspillet mellem guldnanopartikler og celleoverflader for at skabe nye sensorer. Forskelligt formede guldnanopartikler som de -
 Forskere udvikler materiale, der kan regenerere tandemaljenNærbillede af det emaljeagtige materiale. Kredit:Alvaro Mata Forskere ved Queen Mary University of London har udviklet en ny måde at dyrke mineraliserede materialer på, som kan regenerere hårdt væ
Forskere udvikler materiale, der kan regenerere tandemaljenNærbillede af det emaljeagtige materiale. Kredit:Alvaro Mata Forskere ved Queen Mary University of London har udviklet en ny måde at dyrke mineraliserede materialer på, som kan regenerere hårdt væ -
 Skjulte forvrængninger udløser lovende termoelektrisk egenskabBrookhaven Lab-medlemmer af forskerholdet:Simon Billinge, Milinda Abeykoon og Emil Bozin justerer instrumenter til dataindsamling ved parfordelingsfunktionens beamline af National Synchrotron Light So
Skjulte forvrængninger udløser lovende termoelektrisk egenskabBrookhaven Lab-medlemmer af forskerholdet:Simon Billinge, Milinda Abeykoon og Emil Bozin justerer instrumenter til dataindsamling ved parfordelingsfunktionens beamline af National Synchrotron Light So
- Instruktioner fra DNA oversættes til proteiner af organeller kaldet hvad?
- Bedre nano -billeder drejer vejen til forbedret magnetisk hukommelse
- Det iøjnefaldende fravær af kvinder i Indiens arbejdsstyrke
- Hvad er hastigheden på radiofrekvensen?
- Hvad er tilpasninger af en bat?
- Hvilken organelle holder kernen sammen?


