Tin(IV)oxid (SnO2):Ionisk eller kovalent karakter?
* Elektronegativitetsforskel: Tin (Sn) har en elektronegativitet på 1,96, mens oxygen (O) har en elektronegativitet på 3,44. Forskellen i elektronegativitet er stor (1,48), hvilket indikerer, at oxygen stærkt tiltrækker de delte elektroner i bindingen. Dette resulterer i, at ilt får en delvis negativ ladning og tin får en delvis positiv ladning.
* Metal og ikke-metal: Tin er et metal, og ilt er et ikke-metal. Metal-ikke-metalbindinger er typisk ioniske.
* Krystalstruktur: SnO₂ har en krystalstruktur, der ligner rutil (TiO₂), hvor tinionerne er omgivet af oxygenioner i et tetraedrisk arrangement. Denne struktur er i overensstemmelse med ionbinding.
Opsummering: Den store elektronegativitetsforskel, tilstedeværelsen af et metal og et ikke-metal og krystalstrukturen peger alle på, at SnO₂ er en ionisk forbindelse.
Sidste artikelIoniske forbindelser:Rollen af metaller og ikke-metaller
Næste artikelBeregning af atomer i glukose (C6H12O6):En simpel guide
 Varme artikler
Varme artikler
-
 Infrarød sensor fungerer som et nyt værktøj til opdagelse af lægemidlerKredit:Sisacom, Shutterstock Forskere har fundet en ny metode til at analysere, hvordan aktive midler påvirker et specifikt protein, der er vigtigt for celleoverlevelse. Deres forskning kan hjælpe
Infrarød sensor fungerer som et nyt værktøj til opdagelse af lægemidlerKredit:Sisacom, Shutterstock Forskere har fundet en ny metode til at analysere, hvordan aktive midler påvirker et specifikt protein, der er vigtigt for celleoverlevelse. Deres forskning kan hjælpe -
 Pilotskalaanlæg til udvinding af sjældne jordartselementer i hjertet af kullandet(Venstre til højre) Rick Honaker, professor og formand for mineteknik, taler med assisterende forskningsprofessor Wencai Zhang, doktorand Alind Chandra og postdoc Honghu Tang. Kredit:University of Ken
Pilotskalaanlæg til udvinding af sjældne jordartselementer i hjertet af kullandet(Venstre til højre) Rick Honaker, professor og formand for mineteknik, taler med assisterende forskningsprofessor Wencai Zhang, doktorand Alind Chandra og postdoc Honghu Tang. Kredit:University of Ken -
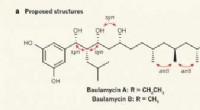 Kemikere udleder den korrekte struktur af A- og B-baulamycinerneTidligere foreslåede og faktiske molekylære strukturer af baulamycinerne. Kredit: Natur (2017). doi:10.1038/nature23265 (Phys.org) – Et team af kemikere ved University of Bristol har korrekt udle
Kemikere udleder den korrekte struktur af A- og B-baulamycinerneTidligere foreslåede og faktiske molekylære strukturer af baulamycinerne. Kredit: Natur (2017). doi:10.1038/nature23265 (Phys.org) – Et team af kemikere ved University of Bristol har korrekt udle -
 Forskere tager røntgenbilleder af elektriske køretøjers batterier, efterhånden som de nedbrydes …Toby Bond justerer en batteriprøve på BMIT-strålelinjen. Kredit:Canadian Light Source Canadian Light Source (CLS) forsker Toby Bond bruger røntgenstråler til at hjælpe med at konstruere kraftfulde
Forskere tager røntgenbilleder af elektriske køretøjers batterier, efterhånden som de nedbrydes …Toby Bond justerer en batteriprøve på BMIT-strålelinjen. Kredit:Canadian Light Source Canadian Light Source (CLS) forsker Toby Bond bruger røntgenstråler til at hjælpe med at konstruere kraftfulde
- Her er, hvad lærere kigger efter, når børn starter i skole
- Målrettede onlineannoncer kan faktisk ændre, hvordan du ser dig selv
- LHCb finder nye antydninger til mulige afvigelser fra standardmodellen
- Hvordan er de fire nukleotider forskellige?
- Hvilken slags overvågningssystem er Gamin?
- Er følelser en form for energi?


