Kulstofbinding:Forståelse af kovalente bindinger og undtagelser
Her er hvorfor:
* Elektronkonfiguration: Kulstof har 4 valenselektroner (elektroner i dens yderste skal). For at opnå en stabil oktet (8 elektroner) skal den få eller dele 4 elektroner mere.
* Kovalent binding: Kulstof opnår denne stabilitet ved at dele sine elektroner med andre atomer gennem kovalente bindinger. Hvert delt elektronpar tæller med i begge atomers oktet.
Undtagelser:
Mens kulstof normalt danner 4 bindinger, er der nogle undtagelser:
* Carbocations: Disse er positivt ladede kulstofioner, der kun danner tre bindinger på grund af tabet af en elektron.
* Fri radikaler: Kulstofatomer med en uparret elektron danner også kun tre bindinger.
* Visse usædvanlige molekyler: Nogle meget reaktive eller ustabile molekyler kan involvere kulstof med mindre end fire bindinger, men disse er ikke almindelige.
Opsummering: Kulstof danner normalt fire kovalente bindinger, men der er nogle specifikke omstændigheder, hvor det kan danne tre.
Sidste artikelFysisk vs. kemisk ændring:Forståelse af blandinger
Næste artikelFluor vs. Brom Atomradius:Hvilken er større?
 Varme artikler
Varme artikler
-
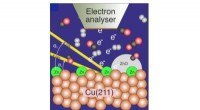 Forskere optrævler den aktive fase i katalytisk kuldioxidreduktion til methanolFigur illustrerer en Cu-overflade dækket med en lille mængde Zn, der er probet med fotoelektronspektroskopi under reaktion af CO2, CO og H2 til methanol. Kredit:Stockholm Universitet Forskere ved S
Forskere optrævler den aktive fase i katalytisk kuldioxidreduktion til methanolFigur illustrerer en Cu-overflade dækket med en lille mængde Zn, der er probet med fotoelektronspektroskopi under reaktion af CO2, CO og H2 til methanol. Kredit:Stockholm Universitet Forskere ved S -
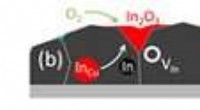 Spørgsmål og svar:Mod en ny måde at producere solceller påKredit:University of Luxembourg Fysikere fra University of Luxembourg sammen med internationale forskere har undersøgt oxidationsprocessen af solcellematerialer, hvis resultater kan ændre den nu
Spørgsmål og svar:Mod en ny måde at producere solceller påKredit:University of Luxembourg Fysikere fra University of Luxembourg sammen med internationale forskere har undersøgt oxidationsprocessen af solcellematerialer, hvis resultater kan ændre den nu -
 Sådan identificeres slutpunktet for en titrering:En trin-for-trin-vejledningAf John Brennan | Opdateret 24. marts 2022 Den mest pålidelige måde at bestemme, hvornår en titrering har nået sit endepunkt, er ved at bruge en pH-indikator. Til syre-basetitreringer ændrer almindel
Sådan identificeres slutpunktet for en titrering:En trin-for-trin-vejledningAf John Brennan | Opdateret 24. marts 2022 Den mest pålidelige måde at bestemme, hvornår en titrering har nået sit endepunkt, er ved at bruge en pH-indikator. Til syre-basetitreringer ændrer almindel -
 Forskere tester nyt materiale til neurocomputereAndrei Ivanov, Lektor i Solid-State Physics and Nanosystems Department ved MEPhI. Kredit:MEPhI Forskere fra National Research Nuclear University MEPhI (Moscow Engineering Physics Institute), arbej
Forskere tester nyt materiale til neurocomputereAndrei Ivanov, Lektor i Solid-State Physics and Nanosystems Department ved MEPhI. Kredit:MEPhI Forskere fra National Research Nuclear University MEPhI (Moscow Engineering Physics Institute), arbej
- Hydraulisk brud påvirker spædbørns sundhed negativt
- Hvad er ethyl- og methylalkohol, hvordan de lavede?
- Ion qubits giver et tidligt glimt af detektering af kvantefejl
- 5 3 er lig med hvor mange meter?
- Forklar, hvordan overskydende gødning kan påvirke nedbrydende organismer?
- NASA forsinker Mars-copterflyvningen til teknisk kontrol


