Natriumchloridopløsning:Forståelse af hydrering i vand
Her er en oversigt:
* Ionisk forbindelse: Natriumchlorid er en ionisk forbindelse, hvilket betyder, at den er sammensat af positivt ladede natriumioner (Na+) og negativt ladede chloridioner (Cl-) holdt sammen af elektrostatiske kræfter.
* Polær opløsningsmiddel: Vand er et polært opløsningsmiddel, hvilket betyder, at det har en positiv og negativ ende på grund af den ujævne fordeling af elektroner i molekylet.
* Opløsning: Når natriumchlorid tilsættes vand, omgiver de polære vandmolekyler ionerne. Den positive ende af vandmolekylet (brint) tiltrækkes af de negative chloridioner, og den negative ende af vandmolekylet (ilt) tiltrækkes af de positive natriumioner.
* Hydrering: Denne tiltrækning bryder ionbindingerne, der holder natrium- og chloridionerne sammen. Ionerne er derefter omgivet af vandmolekyler, der danner hydratiserede ioner. Disse hydratiserede ioner er i det væsentlige de ioner, der er omgivet af en kugle af vandmolekyler.
Så mens natriumchlorid selv forsvinder i vandet, er ionerne stadig til stede, bare omgivet af vandmolekyler.
 Varme artikler
Varme artikler
-
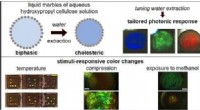 Cellulose:Et altid tilstedeværende materiale med bemærkelsesværdige egenskaberKredit:University of Luxembourg Fysikere fra University of Luxembourg har for nylig taget væsentlige skridt fremad med at løse nogle af de udestående forskningsspørgsmål om cellulose. Deres result
Cellulose:Et altid tilstedeværende materiale med bemærkelsesværdige egenskaberKredit:University of Luxembourg Fysikere fra University of Luxembourg har for nylig taget væsentlige skridt fremad med at løse nogle af de udestående forskningsspørgsmål om cellulose. Deres result -
 Forskere opnår direkte elektrokatalytisk reduktion af kuldioxid, skaber håb om smart kulstofopsaml…CO2 -reduktionsreaktionen finder sted i det katodiske kammer vist til højre. Kredit: Kemisk videnskab Kemikere ved Tokyo Institute of Technology (Tokyo Tech) har foreslået en innovativ måde at op
Forskere opnår direkte elektrokatalytisk reduktion af kuldioxid, skaber håb om smart kulstofopsaml…CO2 -reduktionsreaktionen finder sted i det katodiske kammer vist til højre. Kredit: Kemisk videnskab Kemikere ved Tokyo Institute of Technology (Tokyo Tech) har foreslået en innovativ måde at op -
 Computervision hjælper forskere med at studere lithium-ion-batterierEn ny computervisionsalgoritme til at identificere partikler i en lithium-ion batteri katode har hjulpet forskere med at spore katodens nedbrydning over tid. Kredit:Yijin Liu/SLAC National Accelerator
Computervision hjælper forskere med at studere lithium-ion-batterierEn ny computervisionsalgoritme til at identificere partikler i en lithium-ion batteri katode har hjulpet forskere med at spore katodens nedbrydning over tid. Kredit:Yijin Liu/SLAC National Accelerator -
 Nøjagtig bestemmelse af energiniveauerne for forskellige solceller til højtydende enhedera) Energiniveauer for organiske halvledere målt ved hjælp af UPS, LE-IPES og CV. b,c) Plot, der viser sammenhængen mellem Eoxd og IE (målt via UPS) (b), og Erød og EA (målt via LE-IPES) (c) af donorpo
Nøjagtig bestemmelse af energiniveauerne for forskellige solceller til højtydende enhedera) Energiniveauer for organiske halvledere målt ved hjælp af UPS, LE-IPES og CV. b,c) Plot, der viser sammenhængen mellem Eoxd og IE (målt via UPS) (b), og Erød og EA (målt via LE-IPES) (c) af donorpo


