Delokaliserede Pi-obligationer:Definition, eksempler og betydning
1. Aromatiske forbindelser:
* Benzen: Det klassiske eksempel. De seks carbonatomer danner en ring med skiftende enkelt- og dobbeltbindinger. Imidlertid er pi-elektronerne ikke begrænset til disse individuelle bindinger, men delokaliseres over hele ringen, hvilket skaber en stabil, plan struktur.
* Andre aromatiske systemer: Naphthalen, anthracen, pyridin, furan, thiophen osv., udviser alle lignende delokalisering af deres pi-elektroner i deres ringsystemer.
2. Konjugerede systemer:
* Polyener: Molekyler med skiftende enkelt- og dobbeltbindinger. Pi-elektronerne er delokaliseret over hele det konjugerede system, hvilket gør dem mere stabile end isolerede dobbeltbindinger.
* Carbonylforbindelser: Aldehyder og ketoner har en pi-binding mellem carbon- og oxygenatomerne. Denne pi-binding kan delokaliseres til tilstødende enkeltbindinger, hvis carbonylgruppen er forbundet med en dobbeltbinding eller et system af konjugerede dobbeltbindinger.
3. Visse ioner:
* Carboxylatanioner: Den negative ladning i carboxylater er delokaliseret over begge oxygenatomer, hvilket resulterer i en resonanshybridstruktur.
* Nitratanioner: Den negative ladning er spredt over alle tre iltatomer.
4. Metalkomplekser:
* Ligander: Nogle ligander, som cyclopentadienyl (Cp), kan danne delokaliserede pi-bindinger med metalatomer i organometalliske forbindelser.
Nøgletræk ved delokaliserede Pi-obligationer:
* Øget stabilitet: Delokaliserede pi-bindinger er generelt mere stabile end lokaliserede pi-bindinger på grund af den øgede elektrontæthed i systemet.
* Lavere energi: Delokaliseringen af elektroner sænker den samlede energi af molekylet.
* Forbedret reaktivitet: Delokaliserede pi-bindinger kan deltage i forskellige reaktioner, herunder elektrofil aromatisk substitution, nukleofil addition og Diels-Alder-reaktioner.
At forstå begrebet delokaliserede pi-bindinger er afgørende for at forstå strukturen, egenskaberne og reaktiviteten af en lang række organiske og uorganiske molekyler.
 Varme artikler
Varme artikler
-
 Eksperimentelle fysikere studerer stål om bord på ISSPeter Pichler (tv) med arbejdsgruppeleder Gernot Pottlacher (th.). Fra stålstangen i deres hænder, de skar de små bolde, som nu bliver undersøgt på ISS. Kredit:Baustädter - TU Graz I mange år, Ins
Eksperimentelle fysikere studerer stål om bord på ISSPeter Pichler (tv) med arbejdsgruppeleder Gernot Pottlacher (th.). Fra stålstangen i deres hænder, de skar de små bolde, som nu bliver undersøgt på ISS. Kredit:Baustädter - TU Graz I mange år, Ins -
 Kunstig anti-oxidant kan være det næste supplementGino DiLabio er professor og leder af Institut for Kemi på UBC Okanagan Kredit:UBC Okanagan Naturligt afledte antioxidanter er blevet it sundhedsingrediensen at kigge efter i mad. Men forskere fra
Kunstig anti-oxidant kan være det næste supplementGino DiLabio er professor og leder af Institut for Kemi på UBC Okanagan Kredit:UBC Okanagan Naturligt afledte antioxidanter er blevet it sundhedsingrediensen at kigge efter i mad. Men forskere fra -
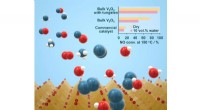 Wolframsubstitueret vanadiumoxid indånder frisk luft i katalysatorteknologiIllustration af ammoniak og nitrogenoxidmolekyler over et krystallinsk katalytisk materiale. (indsat) Kvælstofoxidkonverteringshastigheder ved 150 grader Celsius for wolframsubstitueret bulkvanadiumox
Wolframsubstitueret vanadiumoxid indånder frisk luft i katalysatorteknologiIllustration af ammoniak og nitrogenoxidmolekyler over et krystallinsk katalytisk materiale. (indsat) Kvælstofoxidkonverteringshastigheder ved 150 grader Celsius for wolframsubstitueret bulkvanadiumox -
 Maskinindlæringsmodel forudsiger fænomenets nøgle til forståelse af materielle egenskaberRobert Rudd, Timofey Frolov og Amit Samanta står foran en simulering af de topologiske atomer i et C2H4 -molekyle som defineret af kvanteteorien om atomer i molekyler (QTAIM) og beregnet ved hjælp af
Maskinindlæringsmodel forudsiger fænomenets nøgle til forståelse af materielle egenskaberRobert Rudd, Timofey Frolov og Amit Samanta står foran en simulering af de topologiske atomer i et C2H4 -molekyle som defineret af kvanteteorien om atomer i molekyler (QTAIM) og beregnet ved hjælp af
- Hvad observerede Galileo på Saturn?
- Hvad betyder smeltning i klippecyklussen?
- Hvad er de to typer molekyler, der komponerer cellulære membraner?
- Undersøgelse viser, at avisartikler skifter mening
- Er Jorden en stor eller lille planet-?
- Forskere rekonstruerer sølvhandelen i Middelhavet, fra den trojanske krig til den romerske republik


