Forståelse af intermolekylære kræfter:væsker vs. faste stoffer
* Væsker:
* Stærkere intermolekylære kræfter sammenlignet med gasser. Dette er grunden til, at væsker har et bestemt volumen, men ikke en bestemt form.
* Intermolekylære kræfter overvindes af termisk energi , som tillader molekyler at bevæge sig frit rundt i væsken.
* Faststoffer:
* Meget stærke intermolekylære kræfter , som holder molekyler i en fast, stiv struktur. Dette giver faste stoffer deres bestemte form og volumen.
* Termisk energi er utilstrækkelig at overvinde de stærke intermolekylære kræfter, så molekyler i faste stoffer primært vibrerer omkring faste positioner.
Typer af intermolekylære kræfter:
1. Brintbinding: En særlig stærk type dipol-dipol-interaktion, der opstår mellem et hydrogenatom bundet til et meget elektronegativt atom (som oxygen, nitrogen eller fluor) og et elektronpar på et nærliggende elektronegativt atom.
2. Dipol-dipol-interaktioner: Opstår mellem polære molekyler, der har en permanent positiv og negativ ende (dipol). Disse dipoler justerer sig selv, så den positive ende af et molekyle tiltrækkes af den negative ende af et andet.
3. Spredningskræfter i London: Disse er svage, midlertidige kræfter, der opstår fra midlertidige udsving i elektrontætheden omkring et molekyle. Disse fluktuationer skaber midlertidige dipoler, som inducerer dipoler i tilstødende molekyler. De forekommer mellem alle molekyler, inklusive ikke-polære molekyler.
4. Ioniske kræfter: Opstår i ionforbindelser, hvor der er en stærk elektrostatisk tiltrækning mellem modsat ladede ioner. Disse kræfter er den stærkeste type intermolekylær kraft.
Opsummering: Styrken af de intermolekylære kræfter bestemmer stoffets tilstand. Stærke intermolekylære kræfter er ansvarlige for stivheden af faste stoffer, mens svagere intermolekylære kræfter giver mulighed for flydende væsker.
 Varme artikler
Varme artikler
-
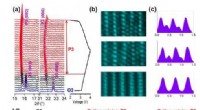 Kationblanding inducerer højeffektiv natriumlagring til lagdelte katoderStrukturel udvikling af NNCT-elektrode under den første cyklus. In-situ XRD-mønstre indsamlet for NNCT-elektrode cyklet i spændingsområdet 2,0-4,0 V (a); STEM-billeder af det uberørte (nederst), fuldt
Kationblanding inducerer højeffektiv natriumlagring til lagdelte katoderStrukturel udvikling af NNCT-elektrode under den første cyklus. In-situ XRD-mønstre indsamlet for NNCT-elektrode cyklet i spændingsområdet 2,0-4,0 V (a); STEM-billeder af det uberørte (nederst), fuldt -
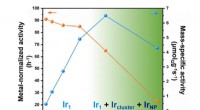 Højbelastende atomisk dispergeret Ir/MoC-katalysator til hydrogeneringsreaktionMetalnormaliseret aktivitet og massespecifik aktivitet af Ir/MoC-katalysatorer med forskelligt Ir-indhold. Ir1 står for atomically dispersed Ir. Skyggen fremhæver, at når Ir -belastningen er lavere en
Højbelastende atomisk dispergeret Ir/MoC-katalysator til hydrogeneringsreaktionMetalnormaliseret aktivitet og massespecifik aktivitet af Ir/MoC-katalysatorer med forskelligt Ir-indhold. Ir1 står for atomically dispersed Ir. Skyggen fremhæver, at når Ir -belastningen er lavere en -
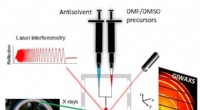 Røntgenstråler afslører in situ krystalvækst af blyfrie perovskit solpanelmaterialerEt skema over den eksperimentelle opsætning, der bruges til at undersøge den strukturelle dannelse af perovskites tynde film under spinbelægning. Kredit:G.Portale, University of Groningen Blybaser
Røntgenstråler afslører in situ krystalvækst af blyfrie perovskit solpanelmaterialerEt skema over den eksperimentelle opsætning, der bruges til at undersøge den strukturelle dannelse af perovskites tynde film under spinbelægning. Kredit:G.Portale, University of Groningen Blybaser -
 Forskerhold opdager, hvordan man konverterer 3D-printet polymer til stærkere, duktilt hybrid-kulsto…De fire hovedtyper af prøver, der er undersøgt i dette arbejde, nemlig som fremstillede, under-carboniserede, delvist carboniserede og over-carboniserede mikrogitter. Kredit:James Utama Surjadi et al.
Forskerhold opdager, hvordan man konverterer 3D-printet polymer til stærkere, duktilt hybrid-kulsto…De fire hovedtyper af prøver, der er undersøgt i dette arbejde, nemlig som fremstillede, under-carboniserede, delvist carboniserede og over-carboniserede mikrogitter. Kredit:James Utama Surjadi et al.
- Hvem var den første person, der så en stjerne i rummet?
- Hvilken gruppe af stjerner kan bruges som et stjerneur til at fortælle tiden om natten?
- Svampe- og insektplanteædere påvirker urtediversiteten afhængigt af artstræk af urter og nabotræ…
- Hvordan månefaser driver havvande
- Hvor lang var Apollo 11 -missionen på måneoverfladen til?
- Hvad er nogle almindelige anvendelser til rhenium?


