Svovlsyre og nikkelreaktion:Forståelse af oxidation
Her er en oversigt:
* Svovlsyre (H₂SO4): Det er en stærk syre, hvilket betyder, at den let donerer hydrogenioner (H+).
* Nikkel (Ni): Det er et metal, og metaller har en tendens til at miste elektroner for at danne positive ioner.
Reaktionen:
Svovlsyre oxiderer nikkel, hvilket betyder, at den fjerner elektroner fra nikkelatomerne. Denne proces danner nikkel(II)-ioner (Ni²⁺) og frigiver brintgas (H₂).
Forenklet reaktion:
Ni(s) + H₂SO4(aq) → NiSO4(aq) + H2(g)
Nøglepunkter:
* Reaktionen er exoterm , hvilket betyder, at den afgiver varme.
* Produktet, nikkelsulfat (NiSO4), er et opløseligt salt, der opløses i den sure opløsning.
* Koncentreret svovlsyre kan bruges til at passivere nikkel, der danner et beskyttende oxidlag på metallets overflade. Denne passiveringsproces gør nikkelen modstandsdygtig over for yderligere korrosion.
Sig til, hvis du har flere spørgsmål.
Sidste artikelEthanol forbrændingsreaktion:Balanceret ligning og forklaring
Næste artikelOxidationstal for iodid (I⁻):En simpel forklaring
 Varme artikler
Varme artikler
-
 Indtageligt medicinsk udstyr kan brydes ned med lysLet nedbrydelige hydrogeler som dynamiske triggere i GI-enheder. (A) Skematisk af ballonindsættelse og inflation (venstre), nedbrydning via enten en endoskopisk eller usammenhængende LED lyskilde (mid
Indtageligt medicinsk udstyr kan brydes ned med lysLet nedbrydelige hydrogeler som dynamiske triggere i GI-enheder. (A) Skematisk af ballonindsættelse og inflation (venstre), nedbrydning via enten en endoskopisk eller usammenhængende LED lyskilde (mid -
 Skeder driver kraftfulde nye kunstige musklerDenne illustration viser et snoet carbon nanorør-garn (CNT) (venstre) og en kappedrevet kunstig muskel (SRAM) fremstillet ved at belægge et snoet CNT-garn med en polymerskede. Et scanningselektronmikr
Skeder driver kraftfulde nye kunstige musklerDenne illustration viser et snoet carbon nanorør-garn (CNT) (venstre) og en kappedrevet kunstig muskel (SRAM) fremstillet ved at belægge et snoet CNT-garn med en polymerskede. Et scanningselektronmikr -
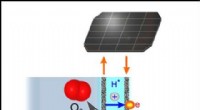 Forskerteamet fører an i et grønt kemi -gennembrud for vedvarende energiElektrolytisk vandopdeling:ilt- og brintudviklingsreaktioner finder sted ved anoden og katoden, som er adskilt af en sur protonledende elektrolyt. Kredit:Monash University Elektrolytisk vandopdeli
Forskerteamet fører an i et grønt kemi -gennembrud for vedvarende energiElektrolytisk vandopdeling:ilt- og brintudviklingsreaktioner finder sted ved anoden og katoden, som er adskilt af en sur protonledende elektrolyt. Kredit:Monash University Elektrolytisk vandopdeli -
 Videnskaben og processen med at udvinde naturgasAf Chris Sherwood, Opdateret 24. marts 2022 Introduktion Naturgas har støt overskygget ældre husholdningers energimuligheder som olie og elektricitet i mange nye og eksisterende boligområder. Dens vo
Videnskaben og processen med at udvinde naturgasAf Chris Sherwood, Opdateret 24. marts 2022 Introduktion Naturgas har støt overskygget ældre husholdningers energimuligheder som olie og elektricitet i mange nye og eksisterende boligområder. Dens vo
- Boligopvarmning topper kilder til PM2,5 i Donau-regionernes byområder
- Online dating bliver mainstream trods nogle tvivl:amerikansk undersøgelse
- Hvilken del af gærcellen omdanner næringsstoffer sukker til energi?
- Pandemikursus forbedrede viden om COVID-19, viser undersøgelse
- Afdækning af et CS Lewis-digt
- Rubiks Cube Science Fair Projekt Idéer


