Forståelse af kuldioxidbindinger:kovalente og polære egenskaber
* Kovalent binding: Kulstof og ilt deler elektroner for at danne bindingen. Denne deling resulterer i en stabil konfiguration for begge atomer.
* Polar: Ilt er mere elektronegativt end kulstof. Dette betyder, at oxygen tiltrækker de delte elektroner stærkere, hvilket skaber en svag negativ ladning (δ-) nær oxygenatomerne og en svag positiv ladning (δ+) nær carbonatomet. Denne ujævne fordeling af ladningen gør bindingen polær.
Vigtig bemærkning: Mens de individuelle C-O-bindinger er polære, er molekylet som helhed lineært og symmetrisk . Det betyder, at polariteterne af de individuelle bindinger ophæver hinanden, hvilket resulterer i et ikke-polært molekyle .
Sidste artikelThiosulfation:Forståelse af polyatomiske ioner og struktur
Næste artikelVandsammensætning:Forståelse af hydrogen og ilt i H₂O
 Varme artikler
Varme artikler
-
 Fremtidens MOF'er:Konvertering af krystallinske metal-organiske rammer til glas eller væskeKrystallinske MOFer bliver nu omdannet til glas/flydende tilstande, åbne nye applikationer. Kredit:Mindy Takamiya Metal-organiske rammer (MOFer) er porøse, krystallinske materialer, der kan fange
Fremtidens MOF'er:Konvertering af krystallinske metal-organiske rammer til glas eller væskeKrystallinske MOFer bliver nu omdannet til glas/flydende tilstande, åbne nye applikationer. Kredit:Mindy Takamiya Metal-organiske rammer (MOFer) er porøse, krystallinske materialer, der kan fange -
 Økologiske krystaller isdannende superkræfterSimuleringer, der viser vandmolekyler (blå) ordnet i et iskrystalgitter (grønt) på forskellige sider af en phloroglucinolkrystal. Kredit:Valeria Molinero/University of Utah I hjertet af skyer er i
Økologiske krystaller isdannende superkræfterSimuleringer, der viser vandmolekyler (blå) ordnet i et iskrystalgitter (grønt) på forskellige sider af en phloroglucinolkrystal. Kredit:Valeria Molinero/University of Utah I hjertet af skyer er i -
 Små broer hjælper partikler med at holde sammenKredit:CC0 Public Domain Det sker uden for dit vindue, hver gang det regner:Jorden bliver våd og kan danne klistret mudder. Så tørrer det. Senere kan det regne igen. Hver befugtning og genfugtning
Små broer hjælper partikler med at holde sammenKredit:CC0 Public Domain Det sker uden for dit vindue, hver gang det regner:Jorden bliver våd og kan danne klistret mudder. Så tørrer det. Senere kan det regne igen. Hver befugtning og genfugtning -
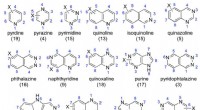 Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114
Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114
- Hvordan bevæger de små molekyler af ilt og kuldioxid sig gennem cellemembranen?
- Skridt landdistrikter kan tage for at beskytte deres vandressourcer
- Hvordan forbedrer man mikroendoskoper? Nyt sondedesign giver løfter om biomedicinsk billeddannelse
- Bliver mere energi reflekteret eller absorberet af jorden?
- Hvad skal der ske med et kromosom, før den næste mitosecyklus starter?
- Hvordan bevæger termisk energi altid?


