Natriumhypochlorit i vand:kemiske reaktioner og biprodukter
1. Hydrolyse:
NaClO + H2O ⇌ HOCl + Na+ + OH-
Denne reaktion involverer hydrolyse af natriumhypochlorit, hvor hypochloritionen (ClO-) reagerer med vand og danner hypochlorsyre (HOCl), natriumioner (Na+) og hydroxidioner (OH-). Denne reaktion er en ligevægtsreaktion, hvilket betyder, at den kan forløbe i begge retninger.
2. Dissociation af hypoklorsyre:
HOCl ⇌ H+ + ClO-
Hypoklorsyre er en svag syre og kan dissociere i vand for at danne hydrogenioner (H+) og hypokloritioner (ClO-). Denne reaktion er også en ligevægtsreaktion.
3. Samlet reaktion:
NaClO + H2O ⇌ HOCl + Na+ + OH- ⇌ H+ + ClO- + Na+ + OH-
Den overordnede reaktion kan forenkles til:
NaClO + H2O ⇌ HOCl + Na+ + OH-
Faktorer, der påvirker ligevægten:
De relative koncentrationer af HOCl, ClO- og OH- i opløsning påvirkes af flere faktorer:
* pH: Opløsningens pH påvirker reaktionernes ligevægt. En lavere pH begunstiger dannelsen af HOCl, mens en højere pH begunstiger dannelsen af ClO-.
* Temperatur: Højere temperaturer øger hastigheden af hydrolysereaktionen, hvilket fører til en højere koncentration af HOCl.
* Koncentration af NaClO: Forøgelse af koncentrationen af NaClO vil øge koncentrationen af HOCl og ClO- i opløsningen.
Betydningen af reaktionerne:
Reaktionerne af natriumhypochlorit i vand er vigtige for dets anvendelse som desinfektionsmiddel og blegemiddel. Hypoklorsyre (HOCl) er et stærkt oxidationsmiddel og er det primære desinfektionsmiddel i opløsninger af natriumhypochlorit. Hydroxidionerne (OH-) bidrager til opløsningens samlede alkalinitet.
Det er vigtigt at bemærke, at de faktiske kemiske reaktioner, der forekommer i vand, er mere komplekse og involverer flere andre faktorer. Ovenstående forklaring giver dog et forenklet overblik over de vigtigste involverede kemiske reaktioner.
 Varme artikler
Varme artikler
-
 Hydrodynamik i cellestudierKredit:IBM I samarbejde med ETH Zürich, vores team hos IBM Research – Zurich udgav en artikel, der gennemgår interaktionen mellem væskestrømme og biologiske celler. Vores arbejde blev vist på fors
Hydrodynamik i cellestudierKredit:IBM I samarbejde med ETH Zürich, vores team hos IBM Research – Zurich udgav en artikel, der gennemgår interaktionen mellem væskestrømme og biologiske celler. Vores arbejde blev vist på fors -
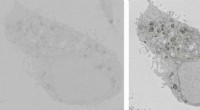 Smart trick muliggør 20 gange hurtigere billeddannelse med elektronmikroskopiTo billeder af en HeLa-celle, begge optaget på 33,6 sekunder. Billedet til højre blev taget, mens en spænding blev påført prøveholderen. Kredit:TU Delft Forskere ved Delft University of Technology
Smart trick muliggør 20 gange hurtigere billeddannelse med elektronmikroskopiTo billeder af en HeLa-celle, begge optaget på 33,6 sekunder. Billedet til højre blev taget, mens en spænding blev påført prøveholderen. Kredit:TU Delft Forskere ved Delft University of Technology -
 Undersøgelse igangsætter kemiske reaktioner ved at afkøle materialer i stedet for at opvarme demKredit:Vanderbilt University En ny undersøgelse foretaget af Vanderbilt-forskere viser evnen til at igangsætte kemiske reaktioner ved at køle materialer i stedet for at opvarme dem - en kontraintui
Undersøgelse igangsætter kemiske reaktioner ved at afkøle materialer i stedet for at opvarme demKredit:Vanderbilt University En ny undersøgelse foretaget af Vanderbilt-forskere viser evnen til at igangsætte kemiske reaktioner ved at køle materialer i stedet for at opvarme dem - en kontraintui -
 Forskere udvikler miljøvenlige, 4-i-1 katalysatorKatalysatorer som denne nye udviklet på Brown University kan muligvis hjælpe med at gøre industriel kemi mere bæredygtig. Kredit:Sun Lab / Seto Lab / Brown University Brown University-forskere har
Forskere udvikler miljøvenlige, 4-i-1 katalysatorKatalysatorer som denne nye udviklet på Brown University kan muligvis hjælpe med at gøre industriel kemi mere bæredygtig. Kredit:Sun Lab / Seto Lab / Brown University Brown University-forskere har
- Opdagelse af en brun dværg dobbeltstjerne med mikrolinsing
- Hvilke ord starter med præfikset bio?
- Forskelle fundet i antioxidantaktiviteter af astaxanthinisomerer mod singlet oxygen
- Hvor meget energi γ-strålefotoner med en bølgelængde på 2.35105 nm?
- Hvad er et miljø, der imødekommer en organismeens behov?
- Hvad sker der, når robotterne lyder for meget som mennesker?


