Beregning af pH af HCl og NaOH-blandinger:En trin-for-trin guide
* Neutraliseringsreaktion: HCl (en stærk syre) og NaOH (en stærk base) reagerer i et molforhold på 1:1 og danner vand (H2O) og salt (NaCl):
HCl + NaOH → H2O + NaCl
* Molaritet og volumen: pH-værdien af den endelige opløsning afhænger af mængden af overskydende syre eller base, der er tilbage efter reaktionen. Dette bestemmes af de indledende volumener af HCl- og NaOH-opløsningerne.
Eksempler på scenarier:
* Lige mængder: Hvis du blander lige store mængder 1N HCl og 1N NaOH, vil opløsningen blive perfekt neutraliseret, hvilket resulterer i en pH på 7 (neutral).
* Mere HCl: Hvis du har mere HCl end NaOH, vil den resulterende opløsning være sur, og pH vil være mindre end 7.
* Mere NaOH: Hvis du har mere NaOH end HCl, vil den resulterende opløsning være basisk, og pH vil være større end 7.
Sådan beregner du pH:
1. Bestem mol HCl og NaOH:
* mol =Molaritet (N) x Volumen (L)
2. Identificer den begrænsende reaktant: Reaktanten med færre mol er den begrænsende reaktant.
3. Beregn antallet af mol af overskydende reaktant: Træk mol af den begrænsende reaktant fra mol af den overskydende reaktant.
4. Beregn koncentrationen af den overskydende reaktant: Del mol af den overskydende reaktant med blandingens samlede volumen.
5. Bestem pH:
* Hvis den overskydende reaktant er HCl:pH =-log[H+]
* Hvis den overskydende reaktant er NaOH:pOH =-log[OH-], så er pH =14 - pOH
Husk: Arbejd altid med volumener i liter (L) for nøjagtige beregninger.
 Varme artikler
Varme artikler
-
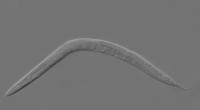 Opdagelsen af livsforlængende vej hos orme viser en ny måde at studere aldring påCaenorhabditis elegans. Kredit:Wikipedia Et enzymblokerende molekyle kan forlænge levetiden for Caenorhabditis elegans rundorme med så meget som 45 procent, hovedsagelig ved at modulere en cannabi
Opdagelsen af livsforlængende vej hos orme viser en ny måde at studere aldring påCaenorhabditis elegans. Kredit:Wikipedia Et enzymblokerende molekyle kan forlænge levetiden for Caenorhabditis elegans rundorme med så meget som 45 procent, hovedsagelig ved at modulere en cannabi -
 Team tager gætterierne ud af at opdage nye legeringer med høj entropiDette er et scanningelektronmikroskops tilbagespredende billede af legeringen Mo/W/Ta/Ti/Zr, med den lysere kontrast (Mo, W, Ta) -baseret fast løsning, mens den mørkere fase er (Ti, Zr) -rig fase. Kre
Team tager gætterierne ud af at opdage nye legeringer med høj entropiDette er et scanningelektronmikroskops tilbagespredende billede af legeringen Mo/W/Ta/Ti/Zr, med den lysere kontrast (Mo, W, Ta) -baseret fast løsning, mens den mørkere fase er (Ti, Zr) -rig fase. Kre -
 Ny algoritme kan hurtigere forudsige LED-materialerForskere fra University of Houston har udtænkt en ny maskinlæringsalgoritme, der er effektiv nok til at køre på en personlig computer og forudsige egenskaberne af mere end 100, 000 forbindelser på jag
Ny algoritme kan hurtigere forudsige LED-materialerForskere fra University of Houston har udtænkt en ny maskinlæringsalgoritme, der er effektiv nok til at køre på en personlig computer og forudsige egenskaberne af mere end 100, 000 forbindelser på jag -
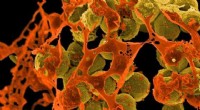 Forskere gør et betydeligt gennembrud på vej mod det nye superbug-dræbende antibiotikum teixobact…Methicillin-resistent Staphylococcus aureus . Kredit:NIH/NIAID Forskere, der arbejder på at udvikle et game-changing nyt antibiotikum, har gjort et betydeligt fremskridt i retning af at skabe ko
Forskere gør et betydeligt gennembrud på vej mod det nye superbug-dræbende antibiotikum teixobact…Methicillin-resistent Staphylococcus aureus . Kredit:NIH/NIAID Forskere, der arbejder på at udvikle et game-changing nyt antibiotikum, har gjort et betydeligt fremskridt i retning af at skabe ko
- Kemikere bruger elektrokemi til at forstærke lægemiddelproduktionen
- Volkswagen satser 15 milliarder euro på elbiler i Kina
- Hvad er 12 og halv sten?
- Hvilke obligationer dannes af tiltrækningen af modsat ladede ioner?
- Hvis et objekt ikke har gemt elastisk energi, hvilken tilstand er den i?
- En islandsk vulkan spyr røde lavastrømme mod en evakueret by


