Hydrogenhalogenidtest:Identifikation og reaktioner
Tests for hydrogenhalogenider:
1. Lakmuspapirtest:
* Sur natur: Hydrogenhalogenider er sure i naturen. De bliver blåt lakmuspapir røde, hvilket indikerer tilstedeværelsen af H+ ioner.
2. Sølvnitrattest:
* Danning af bundfald: Tilsætning af sølvnitrat (AgNO3) opløsning til en hydrogenhalogenidopløsning resulterer i dannelsen af et bundfald, som er et sølvhalogenid (AgX).
* AgCl (sølvchlorid): Hvidt bundfald, uopløseligt i fortyndet salpetersyre.
* AgBr (sølvbromid): Flødefarvet bundfald, let opløseligt i fortyndet salpetersyre.
* AgI (sølviodid): Gult bundfald, praktisk talt uopløseligt i fortyndet salpetersyre.
* Bemærk: Denne test er nyttig til at skelne mellem forskellige halogenider.
3. Reaktion med metaloxider:
* Danning af salt og vand: Hydrogenhalogenider reagerer med metaloxider og danner et salt og vand.
* Eksempel:
* 2HCl + CuO → CuCl2 + H2O
4. Reaktion med metaller:
* Danning af salt og hydrogengas: Hydrogenhalogenider reagerer med aktive metaller for at danne et salt og frigive brintgas.
* Eksempel:
* 2HCl + Zn → ZnCl2 + H2
5. Reaktion med baser:
* Neutralisering: Hydrogenhalogenider reagerer med baser og danner salt og vand.
* Eksempel:
* HCl + NaOH → NaCl + H2O
6. Oxidationsmidler:
* Oxidation til halogener: Stærke oxidationsmidler, såsom kaliumpermanganat (KMnO4) eller kaliumdichromat (K2Cr2O7) i surt medium, kan oxidere hydrogenhalogenider til deres respektive halogener.
* Eksempel:
* 2HCl + KMnO4 + H2SO4 → Cl2 + MnSO4 + K2SO4 + H2O
7. Fysiske egenskaber:
* Rysende: Hydrogenhalogenider (undtagen HF) er røgende gasser på grund af deres høje reaktivitet med fugt i luften.
* Opløselighed: Hydrogenhalogenider er meget opløselige i vand.
8. Specifikke tests for individuelle halogenider:
* HF: Ætser glas på grund af dannelsen af hexafluorsilicationer.
* HCl: Danner hvide dampe af ammoniumchlorid (NH4Cl), når de udsættes for ammoniak.
* HBr: Affarver bromvand på grund af dets reducerende egenskaber.
* HEJ: Affarver kaliumpermanganatopløsning på grund af dens stærke reducerende egenskaber.
Disse tests kan bruges individuelt eller i kombination til at identificere tilstedeværelsen af hydrogenhalogenider og skelne mellem forskellige halogenider.
Sidste artikelKobber- og svovlreaktion:Dannelse af kobbersulfid (CuS)
Næste artikelBinære syrer:Definition, formel, eksempler og egenskaber
 Varme artikler
Varme artikler
-
 Forskere udvikler en optisk fiber fremstillet af gel afledt af havalgerSpiselig, biokompatibel og bionedbrydeligt, disse fibre har potentiale til forskellige medicinske anvendelser. Kredit:Eric Fujiwara En optisk fiber fremstillet af agar er blevet produceret ved Uni
Forskere udvikler en optisk fiber fremstillet af gel afledt af havalgerSpiselig, biokompatibel og bionedbrydeligt, disse fibre har potentiale til forskellige medicinske anvendelser. Kredit:Eric Fujiwara En optisk fiber fremstillet af agar er blevet produceret ved Uni -
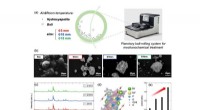 Knogledyb:Mineral fundet i menneskelig knogle kan hjælpe med at bekæmpe giftige organiske forbinde…SEM-billeder afslører, at sammenlignet med løst pakkede partikler i rå HAp, mekanokemisk behandlede HAps viser agglomerater af tætpakkede partikler, hvis størrelse vokser med stigende kuglediameter. I
Knogledyb:Mineral fundet i menneskelig knogle kan hjælpe med at bekæmpe giftige organiske forbinde…SEM-billeder afslører, at sammenlignet med løst pakkede partikler i rå HAp, mekanokemisk behandlede HAps viser agglomerater af tætpakkede partikler, hvis størrelse vokser med stigende kuglediameter. I -
 Illinois forskeres teori om pore-skala transport for at muliggøre forbedret flow batterierAdjunkt Kyle Smith. Kredit:L. Brian Stauffer. Redox-flow-batterier er en ny teknologi til elektrokemisk energilagring, der kan hjælpe med at øge brugen af strøm produceret af vedvarende energire
Illinois forskeres teori om pore-skala transport for at muliggøre forbedret flow batterierAdjunkt Kyle Smith. Kredit:L. Brian Stauffer. Redox-flow-batterier er en ny teknologi til elektrokemisk energilagring, der kan hjælpe med at øge brugen af strøm produceret af vedvarende energire -
 Sådan spores valenselektroner i ioniske forbindelser:En praktisk guideRyan McVay/Photodisc/Getty Images Valenselektronerne er de yderste elektroner, der omgiver et atoms kerne og spiller en afgørende rolle i kemisk binding. I ioniske forbindelser donerer eller accepter
Sådan spores valenselektroner i ioniske forbindelser:En praktisk guideRyan McVay/Photodisc/Getty Images Valenselektronerne er de yderste elektroner, der omgiver et atoms kerne og spiller en afgørende rolle i kemisk binding. I ioniske forbindelser donerer eller accepter
- Synligt gennemsigtig strålingskøler under direkte sollys
- Hvilken type forvitring forekommer granit?
- Hvilken stødende klippe er grønlig sort?
- Hvad skubber mad gennem fordøjelseskanalen?
- Ældre jobansøgere er op til tre gange mindre tilbøjelige til at blive udvalgt til samtale end yng…
- Hvordan arbejdsgivere kan forhindre erfarne ældre arbejdstagere i at gå på pension


