Sådan spores valenselektroner i ioniske forbindelser:En praktisk guide
Ryan McVay/Photodisc/Getty Images
Valenselektronerne er de yderste elektroner, der omgiver et atoms kerne og spiller en afgørende rolle i kemisk binding. I ioniske forbindelser donerer eller accepterer atomer disse elektroner for at opnå en stabil elektronisk konfiguration.
Det periodiske system
På det periodiske system optager ædelgasserne den yderste højre kolonne og besidder fuldstændigt fyldte valensskaller, hvilket gør dem kemisk inerte. Elementer, der støder op til disse gasser, kan let vinde eller miste elektroner for at efterligne den stabile tilstand. For hovedgruppeelementer afspejler gruppenummeret direkte antallet af valenselektroner i deres grundtilstand. For eksempel har et GroupVII-element syv valenselektroner og vil typisk acceptere en elektron i en ionbinding, mens et GroupI-element har en enkelt valenselektron og normalt vil donere det. Dette princip forklarer, hvorfor natrium (Na) mister en elektron for at danne Na⁺, og klor (Cl) får en til at blive Cl⁻ i NaCl.
Ionpolaritet
At kende polariteten af ionerne i en forbindelse giver et hurtigt øjebliksbillede af elektronoverførsel. En positiv ladning indikerer elektrontab, mens en negativ ladning signalerer elektronforstærkning. Ladningens størrelse er lig med antallet af udvekslede elektroner. For eksempel har Ca²⁺ mistet to elektroner under bindingsdannelse.
Elektronegativitet
Elektronegativitet beskriver et atoms tilbøjelighed til at tiltrække elektroner. I et ionpar vil grundstoffet med den højere elektronegativitet normalt acceptere elektroner fra den mindre elektronegative partner. Denne tendens er forudsigelig:Elektronegativitet stiger fra venstre mod højre over en periode og falder fra top til bund.
Oxidationstilstande
Oxidationstilstande repræsenterer de hypotetiske ladninger af atomer i et molekyle. De er uvurderlige til at spore valens-elektronbevægelser. I en neutral ionforbindelse skal summen af alle oxidationstilstande være lig med nul. Som med ionpolaritet angiver en positiv oxidationstilstand elektrontab, og en negativ tilstand betegner elektronforstærkning.
 Varme artikler
Varme artikler
-
 Chokoladens oprindelse:Fra det gamle Sydamerika til moderne fremstillingGustavomellossa/Getty Images Chokolade har udviklet sig fra en ceremoniel bitter væske indtaget af tidlige kulturer til den søde, overbærende godbid, vi nyder i dag. Over fem årtusinder med innovatio
Chokoladens oprindelse:Fra det gamle Sydamerika til moderne fremstillingGustavomellossa/Getty Images Chokolade har udviklet sig fra en ceremoniel bitter væske indtaget af tidlige kulturer til den søde, overbærende godbid, vi nyder i dag. Over fem årtusinder med innovatio -
 Brug af radikaliserede NOₓ-derivater understøttet på metaloxiderGrafisk billede af forskningen. Kredit:Korea Institute of Science and Technology (KIST) INGEN x (X=1 eller 2), der udsendes fra papirvarer/mobilkilder, anses traditionelt for at være berygtede,
Brug af radikaliserede NOₓ-derivater understøttet på metaloxiderGrafisk billede af forskningen. Kredit:Korea Institute of Science and Technology (KIST) INGEN x (X=1 eller 2), der udsendes fra papirvarer/mobilkilder, anses traditionelt for at være berygtede, -
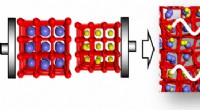 Udnyttelse af geometrisk frustration til at tune batterier for større kraftKredit:ACS En ny generation af kraftigere batterier til telefoner og kameraer kan være resultatet af banebrydende forskning ledet af forskere ved University of Kent. Forskere fra Universitetets S
Udnyttelse af geometrisk frustration til at tune batterier for større kraftKredit:ACS En ny generation af kraftigere batterier til telefoner og kameraer kan være resultatet af banebrydende forskning ledet af forskere ved University of Kent. Forskere fra Universitetets S -
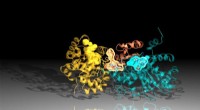 Monkey skruenøgle molekyle syltetøjer tuberkulose proteinBillede af proteinet tryptophansyntase skabt ved hjælp af diffraktionsdata fra Argonnes Advanced Photon Source. Hæmmeren binder sig mellem reaktionsstederne i proteinet, repræsenteret her ved de orang
Monkey skruenøgle molekyle syltetøjer tuberkulose proteinBillede af proteinet tryptophansyntase skabt ved hjælp af diffraktionsdata fra Argonnes Advanced Photon Source. Hæmmeren binder sig mellem reaktionsstederne i proteinet, repræsenteret her ved de orang
- Hvordan er løv?
- Hvilket hav har mange små spredte øer, der blev dannet fra spidserne af uddøde vulkaner?
- Hvad er en produktionsskov?
- Æggekogningsmaskine tilbereder applikationer med kulstof nanorør
- MobiKa:En billig mobilrobot, der kan hjælpe folk i en række forskellige indstillinger
- Når en stråle af lys eneters et medium fra den anden mængde, der aldrig ændrer sig, er det?


