Beregning af mol af ammoniumioner i karbonatforbindelser
1. Identificer forbindelsen:
Du spørger om antallet af ammoniumioner (NH₄⁺) i en prøve af carbonat. Da carbonater indeholder CO₃²⁻-ionen, er vi nødt til at overveje, hvilken ammoniumforbindelse der er tale om. Lad os antage, at du henviser til ammoniumcarbonat ((NH₄)₂CO₃) , som er en almindelig forbindelse.
2. Bestem den molære masse af ammoniumcarbonat:
* Molær masse af (NH₄)₂CO3 =(2 * 14,01 g/mol (N)) + (8 * 1,01 g/mol (H)) + (12,01 g/mol (C)) + (3 * 16,00 g/mol (O))
* Molær masse af (NH₄)₂CO3 =96,09 g/mol
3. Beregn antallet af mol ammoniumcarbonat:
* Mol (NH4)₂CO3 =masse/molmasse
* Mol (NH₄)₂CO3 =8,718 g / 96,09 g/mol
* Mol (NH4)₂CO3 ≈ 0,0907 mol
4. Bestem molforholdet mellem ammoniumioner og ammoniumcarbonat:
* I én formelenhed af (NH₄)₂CO₃ er der to ammoniumioner (NH4+).
* Derfor er molforholdet 2:1.
5. Beregn mol af ammoniumioner:
* Mol NH4⁺ =(mol (NH4)₂CO3) * (2 mol NH4⁺ / 1 mol (NH₄)₂CO₃)
* Mol NH4+ =0,0907 mol * 2
* Mol af NH4⁺ ≈ 0,1814 mol
Derfor er der ca. 0,1814 mol ammoniumioner i 8,718 g ammoniumcarbonat.
Sidste artikelDinitrogenoxid (N₂O) intermolekylære kræfter:hinsides dispersion
Næste artikelpH af alkylhalogenider:Forståelse af neutralitet
 Varme artikler
Varme artikler
-
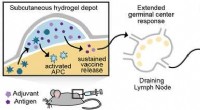 Injicerbar hydrogel kan en dag føre til mere effektive vaccinerKredit:American Chemical Society Vacciner har begrænset spredningen af flere infektionssygdomme, såsom kopper, polio og mæslinger. Imidlertid, vacciner mod visse sygdomme, inklusive HIV-1, influ
Injicerbar hydrogel kan en dag føre til mere effektive vaccinerKredit:American Chemical Society Vacciner har begrænset spredningen af flere infektionssygdomme, såsom kopper, polio og mæslinger. Imidlertid, vacciner mod visse sygdomme, inklusive HIV-1, influ -
 Stabile radikaler kan løse ukonventionelle problemer i moderne videnskab og teknologiPavel Petunin. Kredit:Tomsk Polytechnic Verdazyl-radikaler er stabile molekyler, der indgår i en række organiske stoffer. Du kan bogstaveligt talt fornemme, røre ved, og se dem. Vigtigere, de kan
Stabile radikaler kan løse ukonventionelle problemer i moderne videnskab og teknologiPavel Petunin. Kredit:Tomsk Polytechnic Verdazyl-radikaler er stabile molekyler, der indgår i en række organiske stoffer. Du kan bogstaveligt talt fornemme, røre ved, og se dem. Vigtigere, de kan -
 Nye elektroder kan øge effektiviteten af elektriske køretøjer og flyParaskevi Flouda holder prøve af ny elektrode. Kredit:Texas A&M Engineering Stigningen i popularitet af elektriske køretøjer og fly giver mulighed for at bevæge sig væk fra fossile brændstoffer mo
Nye elektroder kan øge effektiviteten af elektriske køretøjer og flyParaskevi Flouda holder prøve af ny elektrode. Kredit:Texas A&M Engineering Stigningen i popularitet af elektriske køretøjer og fly giver mulighed for at bevæge sig væk fra fossile brændstoffer mo -
 Natriumperborat:Anvendelses-, håndterings- og sikkerhedsvejledningAf Allan Robinson Opdateret 24. marts 2022 Rent natriumperborat (NaBO₃) er et hvidt, lugtfrit fast stof, der typisk krystalliserer med 1, 2 eller 4 vandmolekyler. De kommercielt relevante hydrater –
Natriumperborat:Anvendelses-, håndterings- og sikkerhedsvejledningAf Allan Robinson Opdateret 24. marts 2022 Rent natriumperborat (NaBO₃) er et hvidt, lugtfrit fast stof, der typisk krystalliserer med 1, 2 eller 4 vandmolekyler. De kommercielt relevante hydrater –
- Hvad er afstanden mellem Jorden og Saturn i astronomiske enheder?
- Hvordan bruger et batteri til at tænde din lommelygte demonstrere overførsel af energi?
- Sådan konverteres Watts til Volts
- Kvantificering af strålingsskader i SAXS-eksperimenter
- Hvilken type binding findes mellem aluminium og arsen?
- En omnivore får den energi, den har brug for for at overleve ved?


