Dinitrogenoxid (N₂O) intermolekylære kræfter:hinsides dispersion
Her er hvorfor:
* Molekylær struktur: Dinitrogenoxid har en lineær struktur med oxygenatomet i den ene ende og nitrogenatomerne i den anden. Elektronegativitetsforskellen mellem nitrogen og oxygen skaber en polær binding , hvilket resulterer i et permanent dipolmoment for molekylet.
* Dipol-dipol-interaktioner: På grund af det permanente dipolmoment kan N2O-molekyler interagere med hinanden gennem dipol-dipolkræfter, som er stærkere end dispersionskræfter.
* Spredningskræfter: Mens dipol-dipolkræfter er de dominerende intermolekylære kræfter, er dispersionskræfter også til stede i N2O. Disse kræfter opstår fra midlertidige fluktuationer i elektronfordelingen i molekylet.
Sammenfattende oplever dinitrogenoxid både dipol-dipol-interaktioner og dispersionskræfter, hvor dipol-dipol-kræfter er de væsentligste bidragydere til dets samlede intermolekylære interaktioner.
 Varme artikler
Varme artikler
-
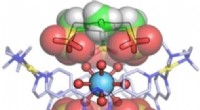 Bur med hætter:Selektiv indeslutning af sjældne jordarters metalhydrater i værtsmolekylerKredit:Wiley Sjældne jordarters metaller er uundværlige i mange tekniske produkter, lige fra smartphones, bærbare computere, batterier, elektromotorer og vindmøller til katalysatorer. I tidsskrifte
Bur med hætter:Selektiv indeslutning af sjældne jordarters metalhydrater i værtsmolekylerKredit:Wiley Sjældne jordarters metaller er uundværlige i mange tekniske produkter, lige fra smartphones, bærbare computere, batterier, elektromotorer og vindmøller til katalysatorer. I tidsskrifte -
 Forskere udvikler en ny proces, der gør affald til kosttilskudNUS-forskerholdet ledet af lektor Yan Ning (til venstre) og adjunkt Zhou Kang (til højre) har udviklet en integreret upcycling-proces til at producere højværdi aminosyrer fra affaldsmaterialer. Kredit
Forskere udvikler en ny proces, der gør affald til kosttilskudNUS-forskerholdet ledet af lektor Yan Ning (til venstre) og adjunkt Zhou Kang (til højre) har udviklet en integreret upcycling-proces til at producere højværdi aminosyrer fra affaldsmaterialer. Kredit -
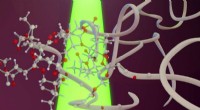 Forskere opdager ny fotoaktiveringsmekanisme til polymerproduktionKredit:Anh Thy Bui Et team af forskere fra North Carolina State University har demonstreret en måde at bruge lavenergi på, synligt lys til fremstilling af polymergelobjekter fra rene monomeropløsn
Forskere opdager ny fotoaktiveringsmekanisme til polymerproduktionKredit:Anh Thy Bui Et team af forskere fra North Carolina State University har demonstreret en måde at bruge lavenergi på, synligt lys til fremstilling af polymergelobjekter fra rene monomeropløsn -
 Smeltning af skrottede enheder, da bæredygtige behov opvarmesKredit:University of Queensland Smeltning af metaller fra kasserede elektroniske enheder er blandt løsninger til bæredygtig forsyning af kritiske materialer, der undersøges af forskere fra Univers
Smeltning af skrottede enheder, da bæredygtige behov opvarmesKredit:University of Queensland Smeltning af metaller fra kasserede elektroniske enheder er blandt løsninger til bæredygtig forsyning af kritiske materialer, der undersøges af forskere fra Univers
- Hvor mange stjerner udgør Constellation Pavo?
- Kinematiske ligninger: Hvornår og hvordan man bruger hver formel (w /derivations)
- Energi kan overføres gennem tomt rum af hvad?
- En skarpere definition af skalafri giver bedre indsigt i netværk
- Hvilket materiale vil lade elektricitet til at strømme mellem et batteri og lysbolb?
- Magma, der tvinger sin vej ind i klipper og hærder kaldes en ekstrudering eller fejl ukonformitet i…


