Elektronegativitet i metaller:Forståelse af tiltrækning og binding
Her er hvorfor:
* Metallisk binding: Metaller danner bindinger, hvor elektroner delokaliseres og deles på tværs af hele strukturen, hvilket gør dem mindre tilbøjelige til at tiltrække elektroner fra andre atomer.
* Elektropositiv karakter: Metaller har en tendens til at miste elektroner og danne positive ioner, hvilket indikerer en lav tiltrækning for elektroner.
Mens nogle metaller har lidt højere elektronegativitet end andre, er de mest elektronegative grundstoffer ikke-metaller såsom fluor (F), oxygen (O), chlor (Cl) og nitrogen (N).
Opsummering: Der er ikke et "mest elektronegativt metal", fordi metaller generelt er elektropositive og har lav elektronegativitet sammenlignet med ikke-metaller.
Sidste artikelSvovlindhold i svovldioxid (SO2):Beregning og procentdel
Næste artikelForståelse af kemiske formler:virkningen af abonnementer
 Varme artikler
Varme artikler
-
 Kemisk syntese kunne producere mere potente antibiotikaKredit:CC0 Public Domain Ved at bruge en ny type kemisk reaktion, MIT-forskere har vist, at de kan modificere antibiotika på en måde, der potentielt kan gøre dem mere effektive mod lægemiddelresis
Kemisk syntese kunne producere mere potente antibiotikaKredit:CC0 Public Domain Ved at bruge en ny type kemisk reaktion, MIT-forskere har vist, at de kan modificere antibiotika på en måde, der potentielt kan gøre dem mere effektive mod lægemiddelresis -
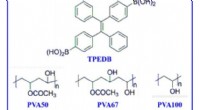 Storskala fremstilling af polymerbaseret stuetemperatur phosphorescens via klikkemiMolekylformler for fosfor og polymermatricer. De molekylære formler for TPEDB, PVA med forskellig alkohollysegrad (PVA50, PVA67, PVA100), og kontrollerede polymerer (PDDA, PSS, og PVDF). Kredit:Scienc
Storskala fremstilling af polymerbaseret stuetemperatur phosphorescens via klikkemiMolekylformler for fosfor og polymermatricer. De molekylære formler for TPEDB, PVA med forskellig alkohollysegrad (PVA50, PVA67, PVA100), og kontrollerede polymerer (PDDA, PSS, og PVDF). Kredit:Scienc -
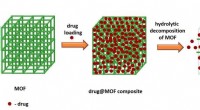 Bare tilsæt vand:Kemikere foreslår en løsning for uopløselige lægemidlerPå billedet er en skematisk repræsentation af et lægemiddel indkapslet i MOF, efterfulgt af den øjeblikkelige frigivelse af lægemidlet fra dets sammensætning. Kredit:Adam Matzger og Suresh Kuruthu
Bare tilsæt vand:Kemikere foreslår en løsning for uopløselige lægemidlerPå billedet er en skematisk repræsentation af et lægemiddel indkapslet i MOF, efterfulgt af den øjeblikkelige frigivelse af lægemidlet fra dets sammensætning. Kredit:Adam Matzger og Suresh Kuruthu -
 Fjernstyret lægemiddeltilførsel implantatstørrelse af druer kan hjælpe med at håndtere kronisk …Fjernstyret, implanterbart nanokanal lægemiddelleveringssystem (nDS) skabt af nanomedicin-forskere ved Houston Methodist Research Institute. Kredit:Houston Methodist Mennesker med kroniske sygdomm
Fjernstyret lægemiddeltilførsel implantatstørrelse af druer kan hjælpe med at håndtere kronisk …Fjernstyret, implanterbart nanokanal lægemiddelleveringssystem (nDS) skabt af nanomedicin-forskere ved Houston Methodist Research Institute. Kredit:Houston Methodist Mennesker med kroniske sygdomm
- Hvad er de to ting, som klimaet består af?
- Sådan sælger du elektricitet tilbage på nettet
- Hvorfor kommunikerer forskere resultaterne af deres forskning?
- Hvad er funktionen af hver plantcelle i specialstrukturen?
- Hvad er et navn på Sea Cliff?
- Dobbelt oprettelse af antimateriale ved hjælp af samme laser energi


