Kemisk syntese kunne producere mere potente antibiotika

Kredit:CC0 Public Domain
Ved at bruge en ny type kemisk reaktion, MIT-forskere har vist, at de kan modificere antibiotika på en måde, der potentielt kan gøre dem mere effektive mod lægemiddelresistente infektioner.
Ved kemisk at forbinde antibiotikummet vancomycin til et antimikrobielt peptid, forskerne var i stand til dramatisk at forbedre lægemidlets effektivitet mod to stammer af lægemiddelresistente bakterier. Denne form for modifikation er enkel at udføre og kan bruges til at skabe yderligere kombinationer af antibiotika og peptider, siger forskerne.
"Typisk, en masse trin ville være nødvendige for at få vancomycin i en form, der ville tillade dig at knytte det til noget andet, men vi behøver ikke at gøre noget ved stoffet, " siger Brad Pentelute, en MIT-lektor i kemi og undersøgelsens seniorforfatter. "Vi blander dem bare sammen, og vi får en konjugationsreaktion."
Denne strategi kan også bruges til at modificere andre typer lægemidler, herunder kræftmedicin, siger Pentelute. At binde sådanne lægemidler til et antistof eller et andet målprotein kan gøre det lettere for lægemidlerne at nå deres tilsigtede destinationer.
Pentelutes laboratorium arbejdede med Stephen Buchwald, Camille Dreyfus professor i kemi ved MIT; Scott Miller, en professor i kemi ved Yale University; og forskere ved Visterra, en lokal biotekvirksomhed, på papiret, som optræder i 5. november-nummeret af Naturkemi . Avisens hovedforfattere er tidligere MIT postdoc Daniel Cohen, MIT postdoc Chi Zhang, og MIT kandidatstuderende Colin Fadzen.
En simpel reaktion
For flere år siden, Cohen gjorde den serendipitiske opdagelse, at en aminosyre kaldet selenocystein spontant kan reagere med komplekse naturlige forbindelser uden behov for en metalkatalysator. Cohen fandt ud af, at da han blandede elektronmangel selenocystein med antibiotikummet vancomycin, selenocysteinet fæstede sig til et bestemt sted - en elektronrig ring af kulstofatomer i vancomycinmolekylet.
Dette fik forskerne til at prøve at bruge selenocystein som et "håndtag", der kunne bruges til at forbinde peptider og lægemidler med små molekyler. De inkorporerede selenocystein i naturligt forekommende antimikrobielle peptider - små proteiner, som de fleste organismer producerer som en del af deres immunforsvar. Selenocystein, en naturligt forekommende aminosyre, der indeholder et selenatom, er ikke så almindelig som de andre 20 aminosyrer, men findes i en håndfuld enzymer i mennesker og andre organismer.
Forskerne fandt ud af, at disse peptider ikke kun var i stand til at forbinde med vancomycin, men de kemiske bindinger forekom konsekvent på samme sted, så alle de resulterende molekyler var identiske. At skabe et sådant rent produkt er vanskeligt med eksisterende metoder til at forbinde komplekse molekyler. Desuden, at udføre denne form for reaktion med tidligere eksisterende metoder ville sandsynligvis kræve 10 til 15 trin bare for at kemisk modificere vancomycin på en måde, der ville tillade det at reagere med et peptid, siger forskerne.
"Det er det smukke ved denne metode, " siger Zhang. "Disse komplekse molekyler har i sig selv regioner, der kan udnyttes til at konjugere til vores protein, hvis proteinet besidder det selenocystein-håndtag, som vi har udviklet. Det kan i høj grad forenkle processen."
Forskerne testede konjugater af vancomycin og en række antimikrobielle peptider (AMP'er). De fandt ud af, at et af disse molekyler, en kombination af vancomycin og AMP dermaseptin, var fem gange stærkere end vancomycin alene mod en bakteriestamme kaldet E. faecalis. Vancomycin knyttet til en AMP kaldet RP-1 var i stand til at dræbe bakterien A. baumannii, selvom vancomycin alene ikke har nogen effekt på denne stamme. Begge disse stammer har høje niveauer af lægemiddelresistens og forårsager ofte infektioner erhvervet på hospitaler.
Modificerede lægemidler
Denne tilgang burde virke for at forbinde peptider til ethvert komplekst organisk molekyle, der har den rigtige slags elektronrig ring, siger forskerne. De har testet deres metode med omkring 30 andre molekyler, herunder serotonin og resveratrol, og fandt ud af, at de let kunne forbindes med peptider indeholdende selenocystein. Forskerne har endnu ikke undersøgt, hvordan disse modifikationer kan påvirke stoffernes aktivitet.
Ud over at modificere antibiotika, som de gjorde i denne undersøgelse, forskerne mener, at de kunne bruge denne teknik til at skabe målrettede kræftlægemidler. Forskere kunne bruge denne tilgang til at binde antistoffer eller andre proteiner til kræftmedicin, hjælper stofferne med at nå deres destination uden at forårsage bivirkninger i sundt væv.
Tilføjelse af selenocystein til små peptider er en ret ligetil proces, siger forskerne, men de arbejder nu på at tilpasse metoden, så den kan bruges til større proteiner. De eksperimenterer også med muligheden for at udføre denne type konjugationsreaktion ved at bruge den mere almindelige aminosyre cystein som håndtag i stedet for selenocystein.
Sidste artikelHudgel tillader sår at hele uden at efterlade et ar
Næste artikelKlar til nærbilledet - en bakteries elektrontransportvej
 Varme artikler
Varme artikler
-
 Power-to-gas anlæg med høj effektivitetDemonstrationsfaciliteten i HELMETH-projektet kombinerer metanering (venstre) og elektrolyse (højre) med en effektivitet på 76 procent. Kredit:sunfire GmbH Naturgasnettet kan fungere som buffer fo
Power-to-gas anlæg med høj effektivitetDemonstrationsfaciliteten i HELMETH-projektet kombinerer metanering (venstre) og elektrolyse (højre) med en effektivitet på 76 procent. Kredit:sunfire GmbH Naturgasnettet kan fungere som buffer fo -
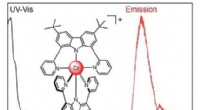 Et nyt kromkompleks udsender lys i uhåndgribelig NIR-II-bølgelængdeKredit:Wiley Mange applikationer, fra fiberoptisk telekommunikation til biomedicinske billeddannelsesprocesser kræver stoffer, der udsender lys i det nær-infrarøde område (NIR). Et forskerhold i S
Et nyt kromkompleks udsender lys i uhåndgribelig NIR-II-bølgelængdeKredit:Wiley Mange applikationer, fra fiberoptisk telekommunikation til biomedicinske billeddannelsesprocesser kræver stoffer, der udsender lys i det nær-infrarøde område (NIR). Et forskerhold i S -
 Flydende kernefibre:En dataflod løber gennem demKernen i den kilometerlange optiske fiber består af glycerin overalt. Kredit:Empa Data og signaler kan overføres hurtigt og pålideligt med glasfibre - så længe fiberen ikke går i stykker. Kraftig
Flydende kernefibre:En dataflod løber gennem demKernen i den kilometerlange optiske fiber består af glycerin overalt. Kredit:Empa Data og signaler kan overføres hurtigt og pålideligt med glasfibre - så længe fiberen ikke går i stykker. Kraftig -
 Ny metode kan føre til bedre in vivo lægemiddelleveringArkivfoto fra Unsplash.com. Kredit:Unsplash.com Credit Badge På et tidspunkt, enhver person vil sandsynligvis opleve en betændelsestilstand. Der er mange årsager til betændelse, og lige så mange b
Ny metode kan føre til bedre in vivo lægemiddelleveringArkivfoto fra Unsplash.com. Kredit:Unsplash.com Credit Badge På et tidspunkt, enhver person vil sandsynligvis opleve en betændelsestilstand. Der er mange årsager til betændelse, og lige så mange b
- Mean tweets og Wall Street:Hvordan Twitter ændrer forsyningskædeovervejelser
- At forstå, hvordan små organiske ioner stabiliserer guldnanopartikler, kan give bedre kontrol
- Kan computerspil hjælpe landmænd med at tilpasse sig klimaforandringerne?
- Undersøgelse undersøger, hvordan billedbøger introducerer børn til politik
- Hvordan andre mennesker påvirker vores interpersonelle rum
- De usikre, ofte rovdyr, verden af kredit i antebellum Virginia


