Molekylær forbindelsesformler:Skal ladninger afbalanceres?
* Molekylære forbindelser dannes af ikke-metaller. Ikke-metaller deler elektroner for at danne kovalente bindinger, hvilket betyder, at de ikke får eller mister elektroner for at danne ioner med positive eller negative ladninger.
* Der er ingen ioner til stede. Da der ingen ioner er, er der ingen ladninger at balancere.
* Formlen afspejler forholdet mellem atomer. De nedskrevne i formlen angiver simpelthen forholdet mellem hvert element i molekylet.
Eksempel:
* Vand (H₂O) har to hydrogenatomer og et oxygenatom. Formlen involverer ikke afbalancering af ladninger, fordi brint- og oxygenatomerne deler elektroner for at danne kovalente bindinger.
Derimod:
* Ioniske forbindelser dannes af metaller og ikke-metaller, som danner ioner med positive og negative ladninger. Disse ladninger *skal* balanceres for at skabe en neutral forbindelse.
Eksempel:
* Natriumchlorid (NaCl) har en natriumion (Na⁺) og en chloridion (Cl⁻). Formlen afspejler balanceringen af +1-ladningen af natrium og -1-ladningen af chlorid.
 Varme artikler
Varme artikler
-
 NIST udvider databasen, der hjælper med at identificere ukendte forbindelser i mælkMichael Power henter en prøve af afrikansk løvemælk fra en fryser. Remoroza vil bringe prøven tilbage til laboratoriet på NIST, hvor hun vil identificere de mange komplekse sukkerarter, kaldet oligosa
NIST udvider databasen, der hjælper med at identificere ukendte forbindelser i mælkMichael Power henter en prøve af afrikansk løvemælk fra en fryser. Remoroza vil bringe prøven tilbage til laboratoriet på NIST, hvor hun vil identificere de mange komplekse sukkerarter, kaldet oligosa -
 Forskere afslører en køreplan for at hjælpe med udvikling af osteoporosebehandlingFra venstre mod højre:forskningsassistent Ruben Garcia-Ordonez, Forskningsassistent Jie Zheng, Professor Pat Griffin, Forskningsassistent Scott Novick, Stabsforsker Mi Ra Chang. Kredit:Scripps Researc
Forskere afslører en køreplan for at hjælpe med udvikling af osteoporosebehandlingFra venstre mod højre:forskningsassistent Ruben Garcia-Ordonez, Forskningsassistent Jie Zheng, Professor Pat Griffin, Forskningsassistent Scott Novick, Stabsforsker Mi Ra Chang. Kredit:Scripps Researc -
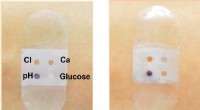 Biosensorbandage opsamler og analyserer svedBiosensorbandage før (venstre) og efter (højre) svedsekretion. Kredit:American Chemical Society Ligesom andre biovæsker, sved indeholder et væld af informationer om, hvad der foregår inde i kroppe
Biosensorbandage opsamler og analyserer svedBiosensorbandage før (venstre) og efter (højre) svedsekretion. Kredit:American Chemical Society Ligesom andre biovæsker, sved indeholder et væld af informationer om, hvad der foregår inde i kroppe -
 Bestemmelse af kemiske egenskaber:En praktisk vejledning til nøjagtig stofidentifikationsfe-co2/iStock/GettyImages Oversigt Identifikation af et stofs kemiske egenskaber er afgørende for sikkerhed, overholdelse og effektiv anvendelse. Ved at udføre systematiske eksperimenter, der udsætt
Bestemmelse af kemiske egenskaber:En praktisk vejledning til nøjagtig stofidentifikationsfe-co2/iStock/GettyImages Oversigt Identifikation af et stofs kemiske egenskaber er afgørende for sikkerhed, overholdelse og effektiv anvendelse. Ved at udføre systematiske eksperimenter, der udsætt


