Oxidationstal for CH2Cl2 (dichlormethan):En detaljeret forklaring
Her er hvorfor:
* Oxidationsnummer repræsenterer den hypotetiske ladning et atom ville have, hvis alle bindinger var 100 % ioniske.
* I et neutralt molekyle , skal summen af alle atomers oxidationstal være lig med nul.
* Brint har typisk et oxidationstal på +1.
* Klor har typisk et oxidationstal på -1.
Lad os nedbryde CH2Cl2:
* Der er to hydrogenatomer (+1 hver) =+2
* Der er to kloratomer (-1 hver) =-2
* Derfor skal kulstofatomet have et oxidationstal på 0 for at balancere molekylet.
Så oxidationstallet for CH2Cl2 er 0.
Sidste artikelVandmolekyler i et mol af is:En simpel beregning
Næste artikelNatrium- og klorioner:Forståelse af ionisk dannelse
 Varme artikler
Varme artikler
-
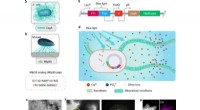 Lysfølsomme E. coli-funktionelle biofilm som stilladser til hydroxyapatitmineraliseringEngineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. Engineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. (a) Skem
Lysfølsomme E. coli-funktionelle biofilm som stilladser til hydroxyapatitmineraliseringEngineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. Engineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. (a) Skem -
 En silica nanostruktur med kemo-enzymatisk opdelingElektronmikrografer af SiJAR (til venstre), elektronmikrografer og fluorescensmikrografer af SiJAR-injicerede celler (til højre). Kredit:POSTECH Da COVID-19-vaccinationer er godt i gang, mennesker
En silica nanostruktur med kemo-enzymatisk opdelingElektronmikrografer af SiJAR (til venstre), elektronmikrografer og fluorescensmikrografer af SiJAR-injicerede celler (til højre). Kredit:POSTECH Da COVID-19-vaccinationer er godt i gang, mennesker -
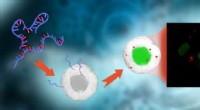 Gennembrud til sporing af RNA med fluorescensKredit:Chalmers University of Technology Forskere ved Chalmers University of Technology, Sverige, det er lykkedes at udvikle en metode til mærkning af mRNA -molekyler, og derved følge, i realtid,
Gennembrud til sporing af RNA med fluorescensKredit:Chalmers University of Technology Forskere ved Chalmers University of Technology, Sverige, det er lykkedes at udvikle en metode til mærkning af mRNA -molekyler, og derved følge, i realtid, -
 Separationsangst ikke mere:En hurtigere teknik til at rense elementer(fra venstre) Rebecca Abergel, Abel Ricano, og Gauthier Deblonde fra Berkeley Labs Chemical Sciences Division har været banebrydende for en hurtigere metode til at rense grundstoffer. Kredit:Marilyn C
Separationsangst ikke mere:En hurtigere teknik til at rense elementer(fra venstre) Rebecca Abergel, Abel Ricano, og Gauthier Deblonde fra Berkeley Labs Chemical Sciences Division har været banebrydende for en hurtigere metode til at rense grundstoffer. Kredit:Marilyn C
- Stort dipolmoment induceret bredspektret bismuthchromat for effektiv fotokatalytisk ydeevne
- Billede:ESA fremdriftslaboratorier testbænk for vandhammer
- Hvilken fysik er involveret, når man skubbes baglæns under start?
- Nanofibersuturer fremmer produktionen af infektionsforhindrende peptid
- En lovende strategi til at øge aktiviteten i antimikrobielle peptider
- Hvornår blev teorien om relativitet fremkaldt?


