Kaustisk soda til at neutralisere saltsyre:Beregning og vejledning
* Koncentration af saltsyren: Dette udtrykkes i enheder som molaritet (mol pr. liter) eller normalitet (ækvivalenter pr. liter).
* Volumen af saltsyren: Dette er mængden af HCl-opløsning, du ønsker at neutralisere.
Sådan beregner du den nødvendige mængde kaustisk soda:
1. Skriv den afbalancerede kemiske ligning:
NaOH + HCl → NaCl + H2O
2. Bestem mol HCl:
* Multiplicer koncentrationen af HCl med volumen af HCl.
* For eksempel, hvis du har 1 liter 1 M HCl, har du 1 mol HCl.
3. Beregn de nødvendige mol NaOH:
* Den afbalancerede ligning viser et 1:1 molforhold mellem NaOH og HCl. Det betyder, at du har brug for det samme antal mol NaOH, som du har mol HCl.
4. Konverter mol NaOH til gram:
* Multiplicer molerne af NaOH med den molære masse af NaOH (40 g/mol).
Eksempel:
Lad os sige, at du har 250 ml 0,5 M HCl og ønsker at neutralisere det med NaOH.
1. Moler HCl: 0,25 L * 0,5 mol/L =0,125 mol HCl
2. Moler NaOH påkrævet: 0,125 mol NaOH
3. Gram NaOH påkrævet: 0,125 mol * 40 g/mol =5 gram NaOH
Vigtig bemærkning: Denne beregning forudsætter fuldstændig neutralisering. I scenarier i den virkelige verden er det ofte bedst at bruge et lille overskud af NaOH for at sikre fuldstændig neutralisering og tage højde for potentielle tab.
Sidste artikelFysisk forandring:Salt og peberblanding forklaret
Næste artikelVandmolekyler i et mol af is:En simpel beregning
 Varme artikler
Varme artikler
-
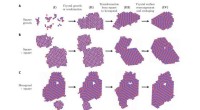 Team opdager, at polymorfe selektion under krystalvækst kan være termodynamisk drevetSnapshots fra MD-simuleringer af selvmontering med interaktionsstyrker EAA/EAB =EBB/EAB =0,15, temperatur kBT/EAB =0,1, og tæthed rs2 =0,1. Eksempler på kvadrat-til-hexagonale transformationer, der fo
Team opdager, at polymorfe selektion under krystalvækst kan være termodynamisk drevetSnapshots fra MD-simuleringer af selvmontering med interaktionsstyrker EAA/EAB =EBB/EAB =0,15, temperatur kBT/EAB =0,1, og tæthed rs2 =0,1. Eksempler på kvadrat-til-hexagonale transformationer, der fo -
 Video:Fremtiden for solcreme begynder med blæksprutteKredit:CC0 Public Domain Pigmenterne i huden på blæksprutter, herunder blæksprutter, blæksprutte, og blæksprutte, kan absorbere ultraviolet stråling. Forskere i Northeasterns Biomaterials Design
Video:Fremtiden for solcreme begynder med blæksprutteKredit:CC0 Public Domain Pigmenterne i huden på blæksprutter, herunder blæksprutter, blæksprutte, og blæksprutte, kan absorbere ultraviolet stråling. Forskere i Northeasterns Biomaterials Design -
 Molybdæntellurid nanoplader muliggør selektiv elektrokemisk produktion af hydrogenperoxid(a) SEM billede af MoTe2 nanoflakes. (b) (nederste panel) Polarisationskurver for MoTe2 -nanoflakes, bulk MoTe2 pulvere og grafen nanoark alene og (øverste panel) tilsvarende ringstrømme (streg linje)
Molybdæntellurid nanoplader muliggør selektiv elektrokemisk produktion af hydrogenperoxid(a) SEM billede af MoTe2 nanoflakes. (b) (nederste panel) Polarisationskurver for MoTe2 -nanoflakes, bulk MoTe2 pulvere og grafen nanoark alene og (øverste panel) tilsvarende ringstrømme (streg linje) -
 Video:Bedre pandekager gennem kemiKredit:The American Chemical Society Alle synes at sværge ved en anden opskrift på pandekage. Hvordan kan du grille de perfekte pandekager til din morgenmad lørdag morgen? Med kemi, selvfølgelig.
Video:Bedre pandekager gennem kemiKredit:The American Chemical Society Alle synes at sværge ved en anden opskrift på pandekage. Hvordan kan du grille de perfekte pandekager til din morgenmad lørdag morgen? Med kemi, selvfølgelig.
- Bybrydende påføring af fugtopfangende film for at reducere varmestress i personlige værnedragter
- Videnskabsprojekter på soda og teeth
- Et nyt spin på livets oprindelse?
- Gør siliciumenheder lydhøre over for infrarødt lys
- Spildevandsnøgle til at løse den globale vandkrise:FN
- To nyere undersøgelser udvider forståelsen af, hvordan tidligt socialt boligbyggeri hjælper malke…


