Redox-reaktioner forklaret:Elektronoverførsel og kemiske processer
Redox-reaktioner:En dans af elektronoverførsel
Kernen i en redoxreaktion ligger overførslen af elektroner mellem reaktanter. Sådan fungerer det:
* Oxidation: En reaktant mister elektroner. Vi siger, at det er blevet *oxideret*. Tænk på det som at miste en negativ ladning, så reaktanten bliver mere positiv.
* Reduktion: En anden reaktant får elektronerne tabt af den første reaktant. Vi siger, at det er blevet *reduceret*. Tænk på det som at få en negativ ladning, så reaktanten bliver mere negativ.
Nøglepunkter
* Altid sammen: Oxidation og reduktion sker altid samtidigt i en redoxreaktion. Du kan ikke have det ene uden det andet.
* LEO siger GER: En praktisk mnemonic at huske:L ose E elektroner O xidation, G ain E elektroner R uddannelse.
Eksempel:Rustning af jern
* Jern (Fe) oxideres: Det mister elektroner for at danne jernioner (Fe²⁺).
* Oxygen (O₂) reduceres: Det får elektronerne tabt af jern og danner oxidioner (O²⁻).
Nøglebegreber
* Oxidationsmiddel: Reaktanten, der får en anden reaktant til at blive oxideret. I rusteksemplet er oxygen oxidationsmidlet.
* Reduktionsmiddel: Den reaktant, der får en anden reaktant til at blive reduceret. Jern er reduktionsmidlet i rusteksemplet.
* Redox-reaktioner i hverdagen: Redoxreaktioner er afgørende for mange processer:
* Åndedræt: Vores kroppe bruger glukose som brændstof og oxiderer det for at frigive energi.
* Fotosyntese: Planter bruger sollys til at omdanne kuldioxid og vand til glukose, en proces, der involverer redoxreaktioner.
* Batterier: Strømmen af elektroner i batterier er et klassisk eksempel på en redoxreaktion.
Sig til, hvis du gerne vil se flere eksempler eller udforske specifikke typer redoxreaktioner. Jeg er her for at hjælpe!
 Varme artikler
Varme artikler
-
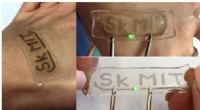 Team udvikler enkel hydrogelmodifikationsmetode mod strækbar og gennemsigtig elektronikSWCNT/hydrogel-baseret mønstret kredsløb afbildet på tre måder:knyttet til menneskelig hud, afslappet, og strakt med 50 pct. Kredit:Skoltech Forskere fra Skolkovo Institute of Science and Technolo
Team udvikler enkel hydrogelmodifikationsmetode mod strækbar og gennemsigtig elektronikSWCNT/hydrogel-baseret mønstret kredsløb afbildet på tre måder:knyttet til menneskelig hud, afslappet, og strakt med 50 pct. Kredit:Skoltech Forskere fra Skolkovo Institute of Science and Technolo -
 Sådan måler du forbrændingsvarmen af paraffinvoks:en trin-for-trin kalorimetrivejledningAf Amber Webb | Opdateret 30. august 2022 MrDamien/iStock/GettyImages I kemi er forbrændingsvarmen kvantificerer den energi, der frigives, når et stof gennemgår fuldstændig oxidation. Bestemmelse af
Sådan måler du forbrændingsvarmen af paraffinvoks:en trin-for-trin kalorimetrivejledningAf Amber Webb | Opdateret 30. august 2022 MrDamien/iStock/GettyImages I kemi er forbrændingsvarmen kvantificerer den energi, der frigives, når et stof gennemgår fuldstændig oxidation. Bestemmelse af -
 Ingeniører viser, hvordan wolframoxid kan bruges som katalysator i bæredygtige kemiske omdannelserEn grafisk gengivelse af nye kemiske katalysatorer, der dukkede op på forsiden af Journal of the American Chemical Association . Kredit:Evan V. Miu Ingeniører er afhængige af katalysatorer til en
Ingeniører viser, hvordan wolframoxid kan bruges som katalysator i bæredygtige kemiske omdannelserEn grafisk gengivelse af nye kemiske katalysatorer, der dukkede op på forsiden af Journal of the American Chemical Association . Kredit:Evan V. Miu Ingeniører er afhængige af katalysatorer til en -
 Funktionaliserede overflader:Cylindriske micellære børster med skræddersyede kemiske muligheder m…Frøet vækst af hydrofobiske PFS53-b-PDMS418 micellære børster på en siliciumwafer. (A) Skematisk illustration af processen, som involverer immobilisering af PFS36-b-P2VP502 frø (Ln =139 nm, Lw/Ln =1,0
Funktionaliserede overflader:Cylindriske micellære børster med skræddersyede kemiske muligheder m…Frøet vækst af hydrofobiske PFS53-b-PDMS418 micellære børster på en siliciumwafer. (A) Skematisk illustration af processen, som involverer immobilisering af PFS36-b-P2VP502 frø (Ln =139 nm, Lw/Ln =1,0
- Hvilke partikler går tabt eller opnås, når de arbejder med statisk elektricitet?
- Team afslører carbon nanorørsjungler for bedre at opdage molekyler
- Hvilke 2 typer partikler findes inden for atomkerner?
- Måneklippen, der viste sig at være fra Jorden
- IQ-test:Kan du forbedre din score ved at øve dig?
- Sådan fungerer skyskrabere


