Sådan måler du forbrændingsvarmen af paraffinvoks:en trin-for-trin kalorimetrivejledning
Af Amber Webb | Opdateret 30. august 2022
MrDamien/iStock/GettyImages
I kemi er forbrændingsvarmen kvantificerer den energi, der frigives, når et stof gennemgår fuldstændig oxidation. Bestemmelse af denne værdi for almindelige brændstoffer - såsom paraffinvoks - giver indsigt i energiomdannelsesprocesser, fra køretøjsmotorer til kalorierne i vores kost. Dette praktiske eksperiment bruger let tilgængelige materialer til at måle forbrændingsvarmen af et paraffinlys, hvilket giver en praktisk forståelse af termokemiske principper.
Eksperimentel procedure
1. Indstil kalorimeteret
Fyld en tom sodavandsdåse med præcis 100 ml koldt vand. Hæng et digitalt termometer i vandet ved hjælp af en stribe Sticky Tack, så det ikke rører dåsens vægge. Dette arrangement udgør et simpelt kalorimeter .
2. Forbered stearinlyset
Klip toppen af en anden sodavandsdåse for at efterlade en 1-2 tommer bred skive. Vej disken og noter dens masse. Vej paraffinlyset, og placer derefter lyset på skiven inde i kalorimeteret.
3. Start forbrænding
Mål den indledende vandtemperatur. Tænd stearinlyset, og løft derefter kalorimeteret med en tang, så flammen er lige over stearinlyset, hvilket sikrer tilstrækkelig luftstrøm. Hold sikker afstand for at undgå forbrændinger.
4. Registrer endelige data
Bemærk den maksimale vandtemperatur, når flammen slukker. Fjern stearinlyset og skiven, vej den resterende stearinlysmasse, og træk skivemassen fra for at opnå massen af voks, der brændte.
Dataanalyse
1. Massebrændt &temperaturstigning
Masse brændt =indledende kyndelmisse – afsluttende kyndelmisse.
ΔT =sluttemperatur – starttemperatur.
2. Termisk energioverførsel
Forudsat 1 ml vand ≈ 1 g, bruger eksperimentet 100 g vand. Vandets specifikke varmekapacitet er 4,18Jg⁻¹°C⁻¹.
Termisk energi (Q) =100g × ΔT × 4,18Jg⁻¹°C⁻¹.
3. Forbrændingsvarme
Forbrændingsvarme (ΔH_comb) =Q ÷ masse forbrændt (g). Resultatet er udtrykt i Jg⁻¹.
Påkrævede materialer
- Paraffinvokslys
- Køligt vand
- To tomme sodavandsdåser
- Tang
- Digitalt termometer (Celsius)
- Sticky Tack
- Nøjagtig balance
- Lettere
Sikkerhedsmeddelelse
Rør ikke ved kalorimeteret, mens det er varmt eller umiddelbart efter. Brug en tang og hold en sikker arbejdsafstand for at forhindre forbrændinger.
Sidste artikelBeregning af kalorimetervarmen (Qcal):En praktisk vejledning
Næste artikelBeregning af et atoms volumen:En praktisk vejledning
 Varme artikler
Varme artikler
-
 Ikke for våd, ikke for tør – plasmabehandlet brændselscelle får det helt rigtigtStudieforfatter Benjamin Zahiri, en materialeforsker Kredit:Benjamin Zahiri Brændselsceller lover som en ren, vedvarende energikilde. Men at holde dem tørre har længe været en udfordring, da de pr
Ikke for våd, ikke for tør – plasmabehandlet brændselscelle får det helt rigtigtStudieforfatter Benjamin Zahiri, en materialeforsker Kredit:Benjamin Zahiri Brændselsceller lover som en ren, vedvarende energikilde. Men at holde dem tørre har længe været en udfordring, da de pr -
 Helikater møder rotaxaner for at skabe løfte om fremtidig sygdomsbehandlingKredit:University of Birmingham En ny tilgang til behandling af kræft og andre sygdomme, der bruger et mekanisk sammenlåst molekyle som en magisk kugle er designet af forskere ved University of Bi
Helikater møder rotaxaner for at skabe løfte om fremtidig sygdomsbehandlingKredit:University of Birmingham En ny tilgang til behandling af kræft og andre sygdomme, der bruger et mekanisk sammenlåst molekyle som en magisk kugle er designet af forskere ved University of Bi -
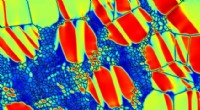 I formhukommelseslegeringer, den rigtige kombination af krystalkorn kan opnå høj styrke og stadig …Simuleret formhukommelsesfaseovergang i en formhukommelseslegering med små og store krystalkorn. Kredit:IOP Publishing A*STAR forskere har vist, gennem en supercomputersimulering, at høj styrke og
I formhukommelseslegeringer, den rigtige kombination af krystalkorn kan opnå høj styrke og stadig …Simuleret formhukommelsesfaseovergang i en formhukommelseslegering med små og store krystalkorn. Kredit:IOP Publishing A*STAR forskere har vist, gennem en supercomputersimulering, at høj styrke og -
 Opdagelsen afdækker behovet for ammoniakudledningsforskrifterDen Europæiske Organisation for Nuklear Forsknings (CERN) skykammer kan genskabe temperaturforhold overalt i atmosfæren, hvilket gør det muligt for forskere at overvåge og analysere partikeldannelse i
Opdagelsen afdækker behovet for ammoniakudledningsforskrifterDen Europæiske Organisation for Nuklear Forsknings (CERN) skykammer kan genskabe temperaturforhold overalt i atmosfæren, hvilket gør det muligt for forskere at overvåge og analysere partikeldannelse i
- Forskere laver justerbare lys-stof-koblinger i nanorør-film
- Hvor krydser jordens rotationsakse med overfladen?
- Intensiteten af stolthed folk føler for en given handling eller egenskab er sat af et implicit me…
- Hvordan er afstanden mellem en planet og solen relateret til dens periodeomdrejning?
- Hvad er processen, der involverer produktion af kemikalier, der hjælper med nedbrydning af mad?
- Frankrig vil søge hårdere tilsyn med 5G-netværksudstyr


