Elektronkonfiguration og kemiske egenskaber:En omfattende vejledning
1. Kemisk binding:
* Valenselektroner og binding: Elektroner i det yderste energiniveau (valenselektroner) er dem, der er involveret i at danne kemiske bindinger med andre atomer.
* Oktetregel: Atomer har tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration med otte valenselektroner (som ædelgasser). Denne drift efter stabilitet er det, der driver kemiske reaktioner.
* Typer af obligationer: Arrangementet af valenselektroner påvirker typen af bindinger atomer danner:
* ioniske bindinger: Et atom mister elektroner og bliver positivt ladet (kation), mens et andet får elektroner og bliver negativt ladet (anion). Disse modsatte ladninger tiltrækker og danner en ionbinding.
* Kovalente bindinger: Atomer deler elektroner for at opnå en stabil konfiguration.
* Metalbindinger: Elektroner er delokaliseret gennem et metalgitter, hvilket skaber et "hav af elektroner", der holder metalatomerne sammen.
2. Reaktivitet:
* Elektronkonfiguration og reaktivitet: Elementer med færre valenselektroner har en tendens til at være mere reaktive, de taber eller deler let elektroner for at opnå stabilitet. Omvendt er elementer med næsten fuld valensskaller mindre reaktive.
* Periodiske tendenser: Det periodiske system organiserer elementer baseret på deres elektronkonfigurationer og hjælper med at forudsige reaktivitet. For eksempel har grundstoffer i samme gruppe (søjle) lignende elektronkonfigurationer og dermed lignende kemiske egenskaber.
3. Kemiske egenskaber:
* Oxidationstilstande: Antallet af elektroner et atom vinder, taber eller deler bestemmer dets oxidationstilstand, hvilket påvirker dets adfærd i kemiske reaktioner.
* Elektronegativitet: Et atoms evne til at tiltrække elektroner i en binding er relateret til dets elektronkonfiguration. Meget elektronegative elementer har tendens til at tiltrække elektroner stærkere, hvilket fører til polære kovalente bindinger.
* Ioniseringsenergi: Den energi, der kræves for at fjerne en elektron fra et atom, bestemmes af styrken af tiltrækningen mellem kernen og elektronen. Dette er påvirket af elektronkonfigurationen og antallet af elektronskaller.
Opsummering:
Ordningen af elektroner i et atom, specifikt valenselektronerne, dikterer, hvordan atomer interagerer med hinanden, danner bindinger og påvirker deres reaktivitet og overordnede kemiske egenskaber. Denne forbindelse mellem elektronkonfiguration og kemiske egenskaber er et grundlæggende princip i kemi, der forklarer mangfoldigheden af kemiske reaktioner og grundstoffernes opførsel.
 Varme artikler
Varme artikler
-
 Riller holder løfte om sofistikeret helbredelseRice University forsker Maryam Elizondo har et 3D-printet stillads graveret med riller til aflejring af levende celler til implantation. Stilladset letter væksten af nye væv, når det nedbrydes. Ved
Riller holder løfte om sofistikeret helbredelseRice University forsker Maryam Elizondo har et 3D-printet stillads graveret med riller til aflejring af levende celler til implantation. Stilladset letter væksten af nye væv, når det nedbrydes. Ved -
 Forskere udvikler banebrydende røntgenteknik til at analysere gamle artefakterFotografier af arkæologiprøverne. Kredit:University of Leicester En banebrydende røntgenteknik, der kan analysere artefakter af enhver form eller tekstur på en ikke-destruktiv måde, er blevet udvi
Forskere udvikler banebrydende røntgenteknik til at analysere gamle artefakterFotografier af arkæologiprøverne. Kredit:University of Leicester En banebrydende røntgenteknik, der kan analysere artefakter af enhver form eller tekstur på en ikke-destruktiv måde, er blevet udvi -
 Konvertering af molaritet (mol/L) til vægtprocent (%):En trin-for-trin guideAf Oxana Fox Opdateret 24. marts 2022 wutwhanfoto/iStock/GettyImages I kemi kan koncentration udtrykkes på mange måder. Molaritet fortæller dig, hvor mange mol af et opløst stof, der er til stede i
Konvertering af molaritet (mol/L) til vægtprocent (%):En trin-for-trin guideAf Oxana Fox Opdateret 24. marts 2022 wutwhanfoto/iStock/GettyImages I kemi kan koncentration udtrykkes på mange måder. Molaritet fortæller dig, hvor mange mol af et opløst stof, der er til stede i -
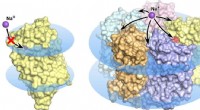 Biofysikere løser den sande struktur af meget lovende optogenetisk protein KR2 rhodopsinKR2 rhodopsin monomer (venstre) og pentamer (højre) i cellemembranen, vist som blå diske. I monomer tilstand, natriumtransport er blokeret, den orange pore tillader ikke ionoptagelse i proteinet. Kred
Biofysikere løser den sande struktur af meget lovende optogenetisk protein KR2 rhodopsinKR2 rhodopsin monomer (venstre) og pentamer (højre) i cellemembranen, vist som blå diske. I monomer tilstand, natriumtransport er blokeret, den orange pore tillader ikke ionoptagelse i proteinet. Kred


