Beregning af pH af en KOH-opløsning:En trin-for-trin guide
1. Beregn mol af KOH:
* Molar masse af KOH: 39,10 g/mol (K) + 16,00 g/mol (O) + 1,01 g/mol (H) =56,11 g/mol
* Moler KOH: (0,140 g KOH) / (56,11 g/mol) =0,00250 mol KOH
2. Beregn koncentrationen af KOH:
* Koncentration (molaritet): (0,00250 mol KOH) / (0,250 L opløsning) =0,0100 M KOH
3. Forstå dissociationen af KOH:
* KOH er en stærk base, hvilket betyder, at den dissocierer fuldstændigt i vand:
KOH(aq) → K+(aq) + OH-(aq)
* Dette betyder, at koncentrationen af OH-ioner er lig med koncentrationen af KOH.
4. Beregn pOH:
* pOH: -log[OH-] =-log(0,0100) =2,00
5. Beregn pH:
* pH + pOH =14
* pH =14 - pOH =14 - 2,00 =12,00
Derfor er opløsningens pH 12,00.
 Varme artikler
Varme artikler
-
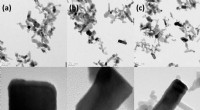 Ingeniører finder en smart måde at omdanne affaldskuldioxid til nyttigt materialeHR-TEM billeder for (a) ZnO-5, (b) ZnO-7 og (c) ZnO-9. Kredit: Avancerede energimaterialer (2020). DOI:10.1002/aenm.202001381 Kemiske ingeniører fra UNSW Sydney har udviklet ny teknologi, der hjæ
Ingeniører finder en smart måde at omdanne affaldskuldioxid til nyttigt materialeHR-TEM billeder for (a) ZnO-5, (b) ZnO-7 og (c) ZnO-9. Kredit: Avancerede energimaterialer (2020). DOI:10.1002/aenm.202001381 Kemiske ingeniører fra UNSW Sydney har udviklet ny teknologi, der hjæ -
 Video:Whiskys kemiKredit:The American Chemical Society Derby Day er rundt om hjørnet, og med det kommer store hatte, heste med sjove navne, og bourbon. Den seneste episode af Reactions fejrer den kemiske destillati
Video:Whiskys kemiKredit:The American Chemical Society Derby Day er rundt om hjørnet, og med det kommer store hatte, heste med sjove navne, og bourbon. Den seneste episode af Reactions fejrer den kemiske destillati -
 Mønstergenkendelse af kemiske bølger i Belousov-Zhabotinsky kemiske reaktionDeres projekt involverede den kemiske reaktion Belousov-Zhabotinsky-et eksempel på en kemisk oscillator, der ofte bruges til at illustrere et kaotisk system. Kredit:University of Exeter Et kollabo
Mønstergenkendelse af kemiske bølger i Belousov-Zhabotinsky kemiske reaktionDeres projekt involverede den kemiske reaktion Belousov-Zhabotinsky-et eksempel på en kemisk oscillator, der ofte bruges til at illustrere et kaotisk system. Kredit:University of Exeter Et kollabo -
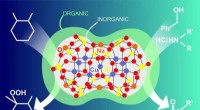 Kemikere syntetiserer en ny hybrid organisk-uorganisk katalysatorKredit:Natalia Deryugina RUDN -kemikere har syntetiseret metalkomplekser på basis af det organoelementale stof silsesquioxan, der består af en organisk og en uorganisk del. Sådanne hybridsystemer
Kemikere syntetiserer en ny hybrid organisk-uorganisk katalysatorKredit:Natalia Deryugina RUDN -kemikere har syntetiseret metalkomplekser på basis af det organoelementale stof silsesquioxan, der består af en organisk og en uorganisk del. Sådanne hybridsystemer
- Hvad er fem egenskaber ved gasser?
- Ideel gaslov:Forståelse af gasadfærd og formel
- Hvad hedder bølgen, der kræver stof for at bære energi?
- Tegn på søvn ses hos vandmænd
- Kunstig intelligens til at forbedre kombinationsdesign og personlig medicin
- Hvad er det hvide på min påskechokolade, og kan jeg stadig spise det?


