Ideel gaslov:Forståelse af gasadfærd og formel
* Tryk (P): Den kraft, som gasmolekylerne udøver på væggene i deres beholder.
* Lydstyrke (V): Den plads, der optages af gassen.
* Temperatur (T): Et mål for den gennemsnitlige kinetiske energi af gasmolekylerne.
* Mængde af gas (n): Normalt målt i mol.
Den ideelle gaslov er repræsenteret ved følgende ligning:
PV =nRT
Hvor:
* R er den ideelle gaskonstant, en værdi, der gør rede for forholdet mellem de andre variable.
Nøgleantagelser for den ideelle gaslov:
* Gasmolekyler har ingen volumen: Det betyder, at molekylerne anses for at være punktmasser med ubetydelig størrelse sammenlignet med den plads, de optager.
* Gasmolekyler interagerer ikke med hinanden: Dette indebærer, at der ikke er nogen tiltrækkende eller frastødende kræfter mellem dem.
* Kollisioner mellem gasmolekyler og beholdervæggene er perfekt elastiske: Det betyder, at der ikke går tabt kinetisk energi under kollisioner.
Ideel adfærd vs. reel adfærd:
Mens den ideelle gaslov giver en nyttig ramme til at forstå gasadfærd, afviger virkelige gasser fra ideel adfærd under visse forhold, såsom:
* Højtryk: Ved høje tryk er gasmolekylerne tættere på hinanden, og deres volumen bliver betydelig sammenlignet med den plads, de optager.
* Lav temperatur: Ved lave temperaturer bliver de tiltrækkende kræfter mellem gasmolekyler mere signifikante, hvilket fører til afvigelser fra ideel adfærd.
På trods af disse afvigelser forbliver den ideelle gaslov et stærkt værktøj til at forudsige og forklare gassers adfærd under mange forhold.
 Varme artikler
Varme artikler
-
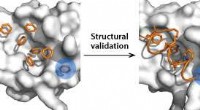 Benzen-baserede prober fremhæver to skjulte bindingssteder på et anticancer-lægemiddelmålBindingslommedetektion ved hjælp af benzenmolekyler som prober (venstre) og strukturel validering ved brug af hæftede peptider (højre). Kredit:Y. S. Tan et al. I jagten på nye kræftbehandlinger, A
Benzen-baserede prober fremhæver to skjulte bindingssteder på et anticancer-lægemiddelmålBindingslommedetektion ved hjælp af benzenmolekyler som prober (venstre) og strukturel validering ved brug af hæftede peptider (højre). Kredit:Y. S. Tan et al. I jagten på nye kræftbehandlinger, A -
 Forskere udvikler unikke materialer til at reparere beskadigede organer og vævForskere skabte biokompatible og bioresorberbare polymermaterialer. Kredit:Peter den Store St. Petersborg Polytekniske Universitet Vævsteknologi er fremtiden for medicin. Polymer Materials for Tis
Forskere udvikler unikke materialer til at reparere beskadigede organer og vævForskere skabte biokompatible og bioresorberbare polymermaterialer. Kredit:Peter den Store St. Petersborg Polytekniske Universitet Vævsteknologi er fremtiden for medicin. Polymer Materials for Tis -
 Lab afslører hjerte-på-en-chipGennem hjerte-på-en-chip-teknologi - modellering af et menneskeligt hjerte på en konstrueret chip og måling af virkningerne af forbindelseseksponering ved hjælp af mikroelektroder - håber Lawrence Liv
Lab afslører hjerte-på-en-chipGennem hjerte-på-en-chip-teknologi - modellering af et menneskeligt hjerte på en konstrueret chip og måling af virkningerne af forbindelseseksponering ved hjælp af mikroelektroder - håber Lawrence Liv -
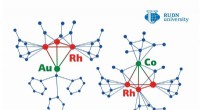 Kemikere foreslår en metode til fremstilling af metalbaserede katalysatorer med uovertruffen effekt…Kredit:RUDN Universitet Et team af kemikere fra RUDN University og Nesmeyanov Institute of Organoelement Compounds (INEOS) syntetiserede to heterometalliske klynger med næsten 100 % effektivitet.
Kemikere foreslår en metode til fremstilling af metalbaserede katalysatorer med uovertruffen effekt…Kredit:RUDN Universitet Et team af kemikere fra RUDN University og Nesmeyanov Institute of Organoelement Compounds (INEOS) syntetiserede to heterometalliske klynger med næsten 100 % effektivitet.


