Beregning af H2SO4-volumen til LiOH-neutralisering:En trin-for-trin guide
1. Skriv den afbalancerede kemiske ligning:
H2SO4(aq) + 2LiOH(aq) → Li2SO4(aq) + 2H2O(l)
2. Beregn mol LiOH:
* Molær masse af LiOH =6,941 g/mol + 15,999 g/mol + 1,008 g/mol =23,948 g/mol
* Mol LiOH =(7,2280 g) / (23,948 g/mol) =0,3018 mol
3. Bestem molforholdet ud fra den balancerede ligning:
* Ligningen viser, at 1 mol H₂SO4 reagerer med 2 mol LiOH.
4. Beregn det nødvendige antal mol H₂SO4:
* Mol H2SO4 =(0,3018 mol LiOH) / (2 mol LiOH/mol H2SO4) =0,1509 mol H2SO4
5. Beregn rumfanget af H₂SO4-opløsning:
* Volumen =mol / molaritet
* Volumen =(0,1509 mol) / (4,494 M) =0,0336 L
Derfor skal du bruge 0,0336 liter (eller 33,6 mL) af 4,494 M H₂SO4-opløsningen for at nå ækvivalenspunktet med 7,2280 g LiOH.
 Varme artikler
Varme artikler
-
 Mikrobielle cyborgs:Bakterier, der leverer strømBakterierne (grønne) er indlejret i en komposit fremstillet af carbon nanorør (grå) og silica nanopartikler (violet) sammenvævet med DNA (blå). (Grafik:Niemeyer Lab, KIT) Kredit:Grafik:Niemeyer Lab, K
Mikrobielle cyborgs:Bakterier, der leverer strømBakterierne (grønne) er indlejret i en komposit fremstillet af carbon nanorør (grå) og silica nanopartikler (violet) sammenvævet med DNA (blå). (Grafik:Niemeyer Lab, KIT) Kredit:Grafik:Niemeyer Lab, K -
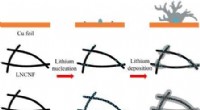 En letvægts nanofiberbaseret opsamlerSkematisk diagram af lithiumkernedannelse og aflejringsadfærd på Cu-folie, lavt nitrogen-dopingniveau carbon nanofiber-ramme og højt nitrogen-doping-niveau carbon-nanofiber-framework. Kredit:©Science
En letvægts nanofiberbaseret opsamlerSkematisk diagram af lithiumkernedannelse og aflejringsadfærd på Cu-folie, lavt nitrogen-dopingniveau carbon nanofiber-ramme og højt nitrogen-doping-niveau carbon-nanofiber-framework. Kredit:©Science -
 Brug af magneter til at kontrollere kemiske reaktioner, der målretter frigivelse af medicin inde i …E- og S-type superparamagnetiske nanopartikler, der bærer enzymet og substratet. en, b, Kryotransmission elektronmikroskopi (cryo-TEM) billede (a) og skematisk (b), der forklarer begrebet magnetfelt-u
Brug af magneter til at kontrollere kemiske reaktioner, der målretter frigivelse af medicin inde i …E- og S-type superparamagnetiske nanopartikler, der bærer enzymet og substratet. en, b, Kryotransmission elektronmikroskopi (cryo-TEM) billede (a) og skematisk (b), der forklarer begrebet magnetfelt-u -
 Ny algoritme afslører cellefabrikkers hemmelighederForskerne testede deres model ved at simulere stofskifte i mere end 300 typer gær. Sammenlignet med målt, allerede eksisterende viden, konkluderede forskerne, at modeller med forudsagte kcat-værdier n
Ny algoritme afslører cellefabrikkers hemmelighederForskerne testede deres model ved at simulere stofskifte i mere end 300 typer gær. Sammenlignet med målt, allerede eksisterende viden, konkluderede forskerne, at modeller med forudsagte kcat-værdier n
- Hvad er de naturlige ressourcer i Samoa?
- Hvorfor er cellecyklussen vigtig for vækst af en organisme?
- Placeringen af ribosomer i en Cell
- Hvorfor er basalt på månen?
- Hvordan er syrer og baser forskellige, hvordan adskiller deres pH -værdier sig?
- Hvilken type kraft kan en magnet udøve på ikke-magnetiske genstande?


