Natriumoxidation:Beregning af elektroner tabt i 42 g natrium
1. Beregn antallet af mol natrium:
* Molær masse af natrium (Na) =22,99 g/mol
* Mol natrium =masse / molær masse =42 g / 22,99 g/mol =1,83 mol
2. Bestem antallet af natriumatomer:
* Avogadros tal =6,022 x 10^23 atomer/mol
* Antal natriumatomer =mol natrium * Avogadros tal =1,83 mol * 6,022 x 10^23 atomer/mol =1,10 x 10^24 atomer
3. Forstå oxidationsprocessen:
* Natrium (Na) mister en elektron for at blive en natriumion (Na+).
4. Beregn det samlede antal tabte elektroner:
* Da hvert natriumatom mister en elektron, er det samlede antal tabte elektroner lig med antallet af natriumatomer.
Derfor mister 42 g natrium 1,10 x 10^24 elektroner, når de oxideres til ioner.
 Varme artikler
Varme artikler
-
 Forskere laver bæredygtig polymer af sukkerarter i træDen nye polymer er fremstillet ved hjælp af xylose, et sukker, der findes i træ. Kredit:Leszek Kobusinski Forskere fra University of Bath har lavet en bæredygtig polymer ved at bruge det næstmest
Forskere laver bæredygtig polymer af sukkerarter i træDen nye polymer er fremstillet ved hjælp af xylose, et sukker, der findes i træ. Kredit:Leszek Kobusinski Forskere fra University of Bath har lavet en bæredygtig polymer ved at bruge det næstmest -
 Nøglen er i belægningen:Flerlagsbelægning for at forbedre korrosionsbestandigheden af stålFlerlagsbelægningen har vist høj modstandsdygtighed over for rust og kan have vidtrækkende konsekvenser på byggeområdet. Kredit:Korea Maritime &Ocean University Stålets styrke gør det til et af de
Nøglen er i belægningen:Flerlagsbelægning for at forbedre korrosionsbestandigheden af stålFlerlagsbelægningen har vist høj modstandsdygtighed over for rust og kan have vidtrækkende konsekvenser på byggeområdet. Kredit:Korea Maritime &Ocean University Stålets styrke gør det til et af de -
 Neutroner forbedrer svejseintegriteten af undervandsvindmøllefundamenterSom vist, den neddykkede buesvejsning har en betydelig bred rille med høje iboende restspændinger. Kredit:DTU/Daniel Sommerlund Pedersen Massive offshore -strukturer som olierigge og vindmøller er
Neutroner forbedrer svejseintegriteten af undervandsvindmøllefundamenterSom vist, den neddykkede buesvejsning har en betydelig bred rille med høje iboende restspændinger. Kredit:DTU/Daniel Sommerlund Pedersen Massive offshore -strukturer som olierigge og vindmøller er -
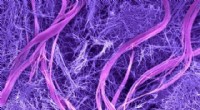 Nye bio-inspirerede dynamiske materialer forvandler sig selvScanningelektronmikrofotografi, der afslører selvsamlede superstrukturer (farvede områder) dannet af den overraskende dynamik af molekyler, der indeholder peptid- og DNA-segmenter. Superstrukturerne e
Nye bio-inspirerede dynamiske materialer forvandler sig selvScanningelektronmikrofotografi, der afslører selvsamlede superstrukturer (farvede områder) dannet af den overraskende dynamik af molekyler, der indeholder peptid- og DNA-segmenter. Superstrukturerne e
- Få Poynting -sætningen til bevarelse af energi i et elektromagnetisk felt?
- Er nordstjernen i Jerusalem?
- Skal førskoleskrivning være mere kommunikation og færre ABC'er?
- Hvad kredserer en stjerne og reflekterer stjernens lys?
- Hvad er trinene, der er involveret i nedbrydning af bjergklipper og deponering af sand silt ler fors…
- Hvad hed metaldelen af blyanten?


