Beregning af produktudbytte i kemiske reaktioner:En støkiometriguide
* Kemiske reaktioner og støkiometri: Kemiske reaktioner følger specifikke forhold mellem reaktanter og produkter. Dette forhold bestemmes af den afbalancerede kemiske ligning for reaktionen.
* Den afbalancerede ligning: Koefficienterne i en afbalanceret kemisk ligning repræsenterer antallet af mol af hvert involveret stof.
* Fuldvarpe og masse: For at relatere massen af reaktanter til massen af produkter, skal du konvertere mellem gram og mol ved hjælp af molmassen af hvert stof.
Her er det, du skal vide for at løse dette problem:
1. Den afbalancerede kemiske ligning: Dette fortæller dig molforholdet mellem reaktanten og produktet.
2. Reaktantens molære masse: Dette konverterer gram reaktant til mol reaktant.
3. Produktets molære masse: Dette konverterer mol produkt til gram produkt.
Eksempel:
Lad os sige, at reaktionen er:
2H2 + O2 -> 2H20
Det betyder, at for hver 2 mol brint (H₂), der reagerer med 1 mol ilt (O₂), producerer du 2 mol vand (H₂O).
Trin til at beregne produktmasse:
1. Konverter gram reaktant til mol:
- Del reaktantens masse (4 gram) med dens molære masse.
2. Brug molforholdet fra den balancerede ligning:
- Bestem antallet af producerede mol produkt baseret på molforholdet i den balancerede ligning.
3. Konverter mol produkt til gram:
- Multiplicer mol af produkt med dets molære masse.
Lad mig vide, hvis du kan give følgende, så kan jeg hjælpe dig med at beregne produktmassen:
* Den afbalancerede kemiske ligning for reaktionen.
* Reaktantens identitet (så vi kan finde dens molære masse).
* Produktets identitet (så vi kan finde dets molære masse).
 Varme artikler
Varme artikler
-
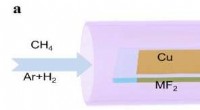 Fluor fremskynder todimensionel materialevækstSkematiske diagrammer over det eksperimentelle design til lokalt at introducere fluor til grafenvækst. Kredit:IBS Tilbage i 2004, fysikfællesskabet var lige begyndt at erkende eksistensen af vir
Fluor fremskynder todimensionel materialevækstSkematiske diagrammer over det eksperimentelle design til lokalt at introducere fluor til grafenvækst. Kredit:IBS Tilbage i 2004, fysikfællesskabet var lige begyndt at erkende eksistensen af vir -
 Hvordan en svamp kan ødelægge immunsystemetSvampen Aspergillus fumigatus er overalt, og er ekstremt farlig for mennesker med svækket immunsystem. Det forekommer stort set overalt på Jorden, som en mørkegrå plet på fugtige vægge eller i mikrosk
Hvordan en svamp kan ødelægge immunsystemetSvampen Aspergillus fumigatus er overalt, og er ekstremt farlig for mennesker med svækket immunsystem. Det forekommer stort set overalt på Jorden, som en mørkegrå plet på fugtige vægge eller i mikrosk -
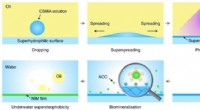 Forskere forbereder Nacre-inspirerede undervands superoleofobiske filmFremstillingsprocedure af den nacre-inspirerede mineraliserede film baseret på superspredning og biomimetisk mineralisering. Kredit:Meng et al. Særlig befugtning af faste overflader er et allesteds
Forskere forbereder Nacre-inspirerede undervands superoleofobiske filmFremstillingsprocedure af den nacre-inspirerede mineraliserede film baseret på superspredning og biomimetisk mineralisering. Kredit:Meng et al. Særlig befugtning af faste overflader er et allesteds -
 Forståelse af flydende egenskaber:definition, adfærd og indvirkning på den virkelige verdenAf Kevin Beck | Opdateret 24. marts 2022 Når vi tænker på en væske, forestiller vi os ofte vand i et glas, et vandløb i en flod eller den glatte overflade af en dam. Alligevel fanger den daglige ople
Forståelse af flydende egenskaber:definition, adfærd og indvirkning på den virkelige verdenAf Kevin Beck | Opdateret 24. marts 2022 Når vi tænker på en væske, forestiller vi os ofte vand i et glas, et vandløb i en flod eller den glatte overflade af en dam. Alligevel fanger den daglige ople
- Djorgovski 2 er en moderat metalfattig kuglehob, undersøgelse finder
- Et strejf salt kan styrke MXene -supermaterialer mod oxidation
- Hvad er de videnskabelige egenskaber til at danne amazonit?
- Undersøgelse modellerer ny metode til at accelerere nanopartikler
- Kvantesimulering kan hjælpe flyvninger til at køre til tiden
- Hvor mange elementer kan ikke findes i naturen?


