Flere kovalente bindinger:definition, typer og eksempler
* Kovalent binding: En binding dannet, når to atomer deler elektroner.
* Flere: Henviser til deling af *mere end ét* elektronpar.
* Typer:
* Dobbeltbinding: To atomer deler to par elektroner (fire elektroner i alt). Repræsenteret af to linjer, der forbinder atomerne i en kemisk struktur.
* Trippelbinding: To atomer deler tre par elektroner (seks elektroner i alt). Repræsenteret af tre linjer, der forbinder atomerne i en kemisk struktur.
Eksempler:
* Oxygen (O2): Iltatomer danner en dobbeltbinding for at opnå en stabil oktet.
* Nitrogen (N2): Nitrogenatomer danner en tredobbelt binding for at opnå en stabil oktet.
* Kuldioxid (CO2): Kulstof danner dobbeltbindinger med hvert oxygenatom.
Egenskaber ved multiple kovalente bindinger:
* Stærkere bånd: Flere bindinger er generelt stærkere end enkeltbindinger, fordi flere elektroner deles, hvilket fører til større elektrostatisk tiltrækning mellem atomerne.
* Kortere bindingslængde: Atomerne holdes tættere sammen på grund af den stærkere tiltrækning.
* Højere bindingsenergi: Der kræves mere energi for at bryde flere bindinger sammenlignet med enkeltbindinger.
Opsummering: Flere kovalente bindinger er afgørende for stabiliteten og funktionaliteten af mange molekyler, hvilket bidrager til deres unikke egenskaber og kemiske reaktivitet.
 Varme artikler
Varme artikler
-
 Konstrueret E. coli kunne lave kulhydrater, vedvarende brændstof, fra CO2Kredit:Pixabay/CC0 Public Domain Forskere fra Newcastle University, UK har konstrueret Escherichia coli bakterier til at opfange kuldioxid (CO 2 ) ved hjælp af brintgas (H 2 ) for at omdanne
Konstrueret E. coli kunne lave kulhydrater, vedvarende brændstof, fra CO2Kredit:Pixabay/CC0 Public Domain Forskere fra Newcastle University, UK har konstrueret Escherichia coli bakterier til at opfange kuldioxid (CO 2 ) ved hjælp af brintgas (H 2 ) for at omdanne -
 Team udvikler meget strækbare hydrogeler til 3D-udskrivning i multimateriale i høj opløsningMeget strækbare og UV -hærdende 3D -print -hydrogeler, der kan strækkes med op til 1300% og er kompatible med højopløselig digital lysbehandlingsbaseret 3D -udskrivning, der muliggør fremstilling af h
Team udvikler meget strækbare hydrogeler til 3D-udskrivning i multimateriale i høj opløsningMeget strækbare og UV -hærdende 3D -print -hydrogeler, der kan strækkes med op til 1300% og er kompatible med højopløselig digital lysbehandlingsbaseret 3D -udskrivning, der muliggør fremstilling af h -
 Første nogensinde in-situ måling af mekaniske egenskaber af hærdet cementmørtel på dybt havTil venstre:Måleapparat ved siden af cementmørtelprøve ved en vanddybde på ca. 3, 500 meter. Til højre:Fjernbetjent køretøj ROV Kaiko Mk-IV, bruges til at installere cementmørtelprøven. Kredit:JAMST
Første nogensinde in-situ måling af mekaniske egenskaber af hærdet cementmørtel på dybt havTil venstre:Måleapparat ved siden af cementmørtelprøve ved en vanddybde på ca. 3, 500 meter. Til højre:Fjernbetjent køretøj ROV Kaiko Mk-IV, bruges til at installere cementmørtelprøven. Kredit:JAMST -
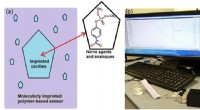 Hurtig påvisning af giftige forbindelserFigur viser (a) princippet for MIP-baserede sensorer, hvor unikke mønstre af målmolekylerne er præget på en polymerbaseret sensorfilm og (b) et eksperiment udføres ved hjælp af den MIP-baserede sensor
Hurtig påvisning af giftige forbindelserFigur viser (a) princippet for MIP-baserede sensorer, hvor unikke mønstre af målmolekylerne er præget på en polymerbaseret sensorfilm og (b) et eksperiment udføres ved hjælp af den MIP-baserede sensor
- Hvad forvandler energi i madkilderne til brugbar energi?
- Hvordan man forstår barometriske tryklæsninger
- Hvis der hverken kan oprettes energi eller ødelægges, hvad sker der med det?
- Ny metode til at producere små revner i elektroder kan betyde et stort løft for nanoelektronikken
- Forskere bruger molekylære lag til at studere varmeoverførsel i nanoskala
- Samarbejde, overvejet:Ny model afslører, hvordan motiver kan påvirke samarbejdet


