Forståelse af regnens surhed:hvorfor det ikke er neutralt
Her er hvorfor:
* CO2 og kulsyre: Når CO2 opløses i vand, danner det kulsyre (H2CO3). Kulsyre er en svag syre, hvilket betyder, at den ikke dissocierer fuldstændigt til ioner i vand. Det bidrager dog til regnvandets surhedsgrad.
* Naturlig pH i regn: pH i rent vand er 7, hvilket er neutralt. Regnvandets naturlige pH er dog typisk omkring 5,6, hvilket gør det let surt. Dette skyldes kulsyren dannet af opløst CO2.
Det er vigtigt at skelne mellem naturlig surhed og sur regn . Sur regn refererer til regn med en pH lavere end 5,6, primært forårsaget af menneskelige aktiviteter som afbrænding af fossile brændstoffer, som frigiver svovldioxid (SO2) og nitrogenoxider (NOx) til atmosfæren. Disse forurenende stoffer reagerer med vand og danner svovlsyre (H2SO4) og salpetersyre (HNO3), hvilket gør regnen betydeligt mere sur.
Så mens regn er naturligt let sur på grund af opløst CO2, refererer udtrykket "sur regn" til regn, der er betydeligt mere sur på grund af menneskeskabt forurening.
Sidste artikelForståelse af dannelsen af vand:ilt- og hydrogenbinding
Næste artikelHydrogenatomer i butan:En kemisk formelnedbrydning
 Varme artikler
Varme artikler
-
 Ingeniører finder, at antioxidanter forbedrer nanoskala visualisering af polymererTilføjelse af antioxidanter kan skubbe opløsningsgrænsen for polymerelektronmikroskopi for at afsløre en struktur, der er mindre i skala (blå) sammenlignet med den struktur, der tidligere er observere
Ingeniører finder, at antioxidanter forbedrer nanoskala visualisering af polymererTilføjelse af antioxidanter kan skubbe opløsningsgrænsen for polymerelektronmikroskopi for at afsløre en struktur, der er mindre i skala (blå) sammenlignet med den struktur, der tidligere er observere -
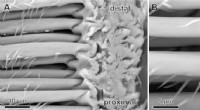 Overraskende opdagelse af edderkoppehår kan inspirere til stærkere klæbemidlerScanning Electron Microscopy (SEM) billede af baserne af pretarsal (dvs. på nederste del af benet) klæbende hår. (A) Til venstre er hårskaftene på de klæbende hår nærmest exoskeleton. Ved deres indsæt
Overraskende opdagelse af edderkoppehår kan inspirere til stærkere klæbemidlerScanning Electron Microscopy (SEM) billede af baserne af pretarsal (dvs. på nederste del af benet) klæbende hår. (A) Til venstre er hårskaftene på de klæbende hår nærmest exoskeleton. Ved deres indsæt -
 Brug af stamme til at kontrollere oxynitrid -egenskaberForskere fandt en måde at oprette og kontrollere retningen og periodiciteten af ilt-ledige lag i oxynitridkrystaller ved en temperatur så lav som 600 ° C. Kredit:Mindy Takamiya/Kyoto University iCeM
Brug af stamme til at kontrollere oxynitrid -egenskaberForskere fandt en måde at oprette og kontrollere retningen og periodiciteten af ilt-ledige lag i oxynitridkrystaller ved en temperatur så lav som 600 ° C. Kredit:Mindy Takamiya/Kyoto University iCeM -
 Valg af den rigtige flaske til opbevaring af syrer og baser:En praktisk vejledningAf Rochelle Leggett Opdateret 24. marts 2022 MadamLead/iStock/GettyImages Stærke syrer og baser udgør væsentlige sundhedsfarer, så valg af den korrekte beholder er afgørende for sikkerheden og over
Valg af den rigtige flaske til opbevaring af syrer og baser:En praktisk vejledningAf Rochelle Leggett Opdateret 24. marts 2022 MadamLead/iStock/GettyImages Stærke syrer og baser udgør væsentlige sundhedsfarer, så valg af den korrekte beholder er afgørende for sikkerheden og over
- Ændrede en useriøs stjerne sammensætningen af vores solsystem?
- Hvor meget vindenergi bruges over hele verden?
- Hvorfor er kuldioxid og nitrogenprodukter, når du forbrænder metan?
- Hvilken enhed opdeler lys?
- Hvor går børn i billige boliger i skole?
- Hvis temperaturen på et objekt er 45C, hvad på Kelvin -skalaen?


