Forståelse af dannelsen af vand:ilt- og hydrogenbinding
1. Elektronegativitet: Ilt er væsentligt mere elektronegativt end brint. Det betyder, at ilt har et stærkere træk på delte elektroner i en binding. Når oxygen og brint bindes, bruger elektronerne mere tid omkring oxygenatomet, hvilket giver det en delvis negativ ladning og brintatomerne en delvis positiv ladning.
2. Oktetregel: Oxygen ønsker at have en fuld ydre skal på otte elektroner. Den har seks elektroner i sin ydre skal. Ved at danne to kovalente bindinger med to hydrogenatomer får den yderligere to elektroner, fuldender dens oktet og opnår stabilitet.
3. Hydrogenbinding: Det resulterende vandmolekyle har en bøjet form på grund af de enlige elektronpar på iltatomet. Dette skaber et polært molekyle med en positiv side (brintatomer) og en negativ side (iltatom). Disse modsatte ladninger tillader vandmolekyler at danne stærke brintbindinger med hinanden, hvilket fører til mange af vands unikke egenskaber.
4. Energifrigivelse: Dannelsen af vand fra ilt og brint frigiver energi, hvilket gør reaktionen gunstig.
Opsummering: Kombinationen af oxygens høje elektronegativitet, dets ønske om at færdiggøre sin oktet, dannelsen af hydrogenbindinger og frigivelsen af energi bidrager alt sammen til den lethed, hvormed oxygenatomer kombineres med to brintatomer for at danne vand.
 Varme artikler
Varme artikler
-
 Innovationspionerer scorer verdens først for bæredygtigt byggeri med grafenbetonTeam fra University of Manchester og Nationwide Engineering om verdens første konstruerede grafenbeton i kommercielle omgivelser, kun et par kilometer øst for det gamle monument i Stonehenge, det nye
Innovationspionerer scorer verdens først for bæredygtigt byggeri med grafenbetonTeam fra University of Manchester og Nationwide Engineering om verdens første konstruerede grafenbeton i kommercielle omgivelser, kun et par kilometer øst for det gamle monument i Stonehenge, det nye -
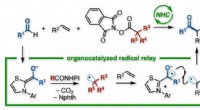 Vicinal reaktion:En radikal strategi for sammenkædning af tre organiske grupperEt japansk forskerteam ved Kanazawa University udviklede en reaktion for at skabe funktionaliserede ketoner. Ved hjælp af en N-heterocyklisk carbene (NHC) organokatalysator, uden behov for metaller el
Vicinal reaktion:En radikal strategi for sammenkædning af tre organiske grupperEt japansk forskerteam ved Kanazawa University udviklede en reaktion for at skabe funktionaliserede ketoner. Ved hjælp af en N-heterocyklisk carbene (NHC) organokatalysator, uden behov for metaller el -
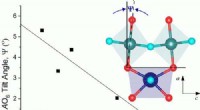 Opbygning af viden om ændringer i urankemiKredit:Australian Nuclear Science and Technology Organisation (ANSTO) Der er stadig rigtig mange spørgsmål, der skal besvares inden for urankemi, især i forbindelse med det nukleare brændselskreds
Opbygning af viden om ændringer i urankemiKredit:Australian Nuclear Science and Technology Organisation (ANSTO) Der er stadig rigtig mange spørgsmål, der skal besvares inden for urankemi, især i forbindelse med det nukleare brændselskreds -
 Beregning af teoretisk udbytte:En praktisk vejledning for kemikereAf Kaylee Finn, Opdateret 30. august 2022 Vicheslav/iStock/GettyImages Teoretisk udbytte er et grundlæggende begreb i kemi, der repræsenterer den maksimale mængde produkt, der kan dannes, når en rea
Beregning af teoretisk udbytte:En praktisk vejledning for kemikereAf Kaylee Finn, Opdateret 30. august 2022 Vicheslav/iStock/GettyImages Teoretisk udbytte er et grundlæggende begreb i kemi, der repræsenterer den maksimale mængde produkt, der kan dannes, når en rea


