Kuldioxid og kalkvandsreaktion:En detaljeret forklaring
Sådan opstår reaktionen:
1. Kalkvand er en klar, farveløs opløsning af calciumhydroxid ($Ca(OH)_2$) i vand.
2. Culdioxid er en farveløs, lugtfri gas.
3. Når kuldioxid bobles gennem kalkvand, opløses det i vandet og reagerer med calciumhydroxidet og danner calciumcarbonat og vand:
$CO_2(g) + Ca(OH)_2(aq) \højrepil CaCO_3(s) + H_2O(l)$
4. Calciumcarbonat er et hvidt, uopløseligt fast stof, der fremstår som et mælkehvidt bundfald i opløsningen. Dette gør, at kalkvandet bliver uklart.
Reaktionen er reversibel:
Hvis du fortsætter med at boble kuldioxid gennem kalkvandet, vil det mælkehvide bundfald til sidst opløses. Dette skyldes, at det overskydende kuldioxid vil reagere med calciumcarbonatet for at danne calciumbicarbonat ($Ca(HCO_3)_2$), som er opløseligt i vand:
$CaCO_3(s) + CO_2(g) + H_2O(l) \højrepil Ca(HCO_3)_2(aq)$
Opsummering:
* Kuldioxid, der reagerer med kalkvand, resulterer i dannelsen af et mælkehvidt bundfald af calciumcarbonat, hvilket er en karakteristisk indikation på tilstedeværelsen af kuldioxid.
* Reaktionen er reversibel, og overskydende kuldioxid kan opløse bundfaldet.
 Varme artikler
Varme artikler
-
 Fremskridt hen imod tilslutning af en antibiotikapumpeSusan Rempe står foran Center for Integrated Nanotechnologies, hvor noget af hendes forskning om bakteriepumper blev lavet. Hendes team fra Sandia National Laboratories og University of Illinois i Urb
Fremskridt hen imod tilslutning af en antibiotikapumpeSusan Rempe står foran Center for Integrated Nanotechnologies, hvor noget af hendes forskning om bakteriepumper blev lavet. Hendes team fra Sandia National Laboratories og University of Illinois i Urb -
 Forskere syntetiserer nye flydende krystaller, der tillader rettet transmission af elektricitetStrukturformlen for flydende krystaller overlejret på et billede af den flydende krystalfase fremstillet ved hjælp af et polariseret lysmikroskop sammen med eksempler på fluorescensen udvist af flyden
Forskere syntetiserer nye flydende krystaller, der tillader rettet transmission af elektricitetStrukturformlen for flydende krystaller overlejret på et billede af den flydende krystalfase fremstillet ved hjælp af et polariseret lysmikroskop sammen med eksempler på fluorescensen udvist af flyden -
 Forskere frigør potentialet i ultratynde 2D-materialerDr. Hieu Nguyen og Ph.D. kandidat Mike Tebyetekerwa. Kredit:Australian National University Forskere fra The Australian National University (ANU) har, for første gang, demonstreret det maksimale po
Forskere frigør potentialet i ultratynde 2D-materialerDr. Hieu Nguyen og Ph.D. kandidat Mike Tebyetekerwa. Kredit:Australian National University Forskere fra The Australian National University (ANU) har, for første gang, demonstreret det maksimale po -
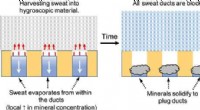 Vende sveden mod sig selv med en metalfri antiperspirantKredit:American Chemical Society Kropslugt er en ubehagelig lugt, produceres, når bakterier, der lever på huden, nedbryder proteinerne i sved. For at undgå at stinke, nogle mennesker anvender anti
Vende sveden mod sig selv med en metalfri antiperspirantKredit:American Chemical Society Kropslugt er en ubehagelig lugt, produceres, når bakterier, der lever på huden, nedbryder proteinerne i sved. For at undgå at stinke, nogle mennesker anvender anti
- Det tidlige univers var et flydende kvark-gluonplasma
- Hvilke kræfter handler på en varmluftsballon?
- Hvorfor er den øverste overflade af et blad gennemsigtigt?
- Kan du rense saltvand med varme?
- Hvor lang tid tager det solen at flytte en grad over under horisonten?
- Bærer kortbølgelængde lys mere energi eller mindre end langbølgelængde lys?


