CO Molekylær Geometri:Forståelse af kulilte's lineære form
Her er hvorfor:
* Lewis-struktur: Lewis-strukturen af CO viser en tredobbelt binding mellem carbon- og oxygenatomerne. Denne tredobbelte binding består af en sigma-binding og to pi-bindinger.
* Hybridisering: Kulstofatomet i CO gennemgår sp-hybridisering, hvilket betyder, at det har to hybridorbitaler. Disse hybridorbitaler peger i modsatte retninger, hvilket resulterer i en lineær geometri.
* Elektrondomæner: Der er to elektrondomæner omkring carbonatomet (den tredobbelte binding med oxygen), og to elektrondomæner omkring oxygenatomet (den tredobbelte binding med kulstof og to ensomme par). Dette understøtter også den lineære form.
Derfor har CO en lineær molekylær form med kulstof- og oxygenatomerne på linje i en lige linje.
 Varme artikler
Varme artikler
-
 Video:Hvad er kemien bag ringorm?Vidste du, at ringorm faktisk ikke er en orm? Denne uge om reaktioner, find ud af hvad ringorm er; hvordan den skyldige lever af din hud, hår og negle; og hvordan man ikke bliver det næste måltid:
Video:Hvad er kemien bag ringorm?Vidste du, at ringorm faktisk ikke er en orm? Denne uge om reaktioner, find ud af hvad ringorm er; hvordan den skyldige lever af din hud, hår og negle; og hvordan man ikke bliver det næste måltid: -
 Genetik indsats beriger ernæring af popcorn, sorghumNebraskas David Holding (til højre) og Leandra Marshall (til venstre) er ved at udvikle linjer af popcorn med højere niveauer af lysin, en aminosyre, der er essentiel for menneskers og nogle husdyrs k
Genetik indsats beriger ernæring af popcorn, sorghumNebraskas David Holding (til højre) og Leandra Marshall (til venstre) er ved at udvikle linjer af popcorn med højere niveauer af lysin, en aminosyre, der er essentiel for menneskers og nogle husdyrs k -
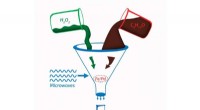 En miljøvenlig metode til syntese af kanelaldehydKredit:RUDN Universitet En kemiker fra RUDN University har udviklet en økologisk sikker metode til at opnå kanelaldehyd - en forbindelse med antibakteriel og anticanceraktivitet. Forskeren brugte
En miljøvenlig metode til syntese af kanelaldehydKredit:RUDN Universitet En kemiker fra RUDN University har udviklet en økologisk sikker metode til at opnå kanelaldehyd - en forbindelse med antibakteriel og anticanceraktivitet. Forskeren brugte -
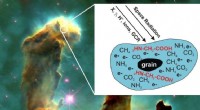 Hvordan livets byggesten kan dannes i rummetElektroner med lav energi skabt i stof af rumstråling (f.eks. galaktiske kosmiske stråler, GCR, etc.), kan inducere dannelse af glycin (2HN-CH2-COOH) i astrofysiske molekylære iser; her, iskolde korn
Hvordan livets byggesten kan dannes i rummetElektroner med lav energi skabt i stof af rumstråling (f.eks. galaktiske kosmiske stråler, GCR, etc.), kan inducere dannelse af glycin (2HN-CH2-COOH) i astrofysiske molekylære iser; her, iskolde korn
- Apples iPad Wi-Fi med 3G:Er adgang til enhver tid det værd?
- Hvilke opløsningsmidler bruges til at opløse kanelaldehyd?
- Hvilken type dannelse bevæger sediment og eroderer rock?
- Verdens mindste radiomodtager har byggesten på størrelse med to atomer
- Skriv en afbalanceret kemisk ligning til fermentering af saccharose af gær, hvor sukker reagerer me…
- Hvad får en halv måne til at dannes på nattehimlen?


