Hvorfor danner atomer ikke forbindelser? Forståelse af kemisk binding
Faktorer, der påvirker forbindelsesdannelse:
* Elektronegativitet: Forskellen i elektronegativitet mellem to atomer bestemmer, hvilken type binding de danner. Store forskelle fører til ionbindinger, mens mindre forskelle fører til kovalente bindinger.
* Ioniseringsenergi: Den energi, der kræves for at fjerne en elektron fra et atom. Lav ioniseringsenergi tyder på, at et atom er mere tilbøjelige til at miste elektroner og blive en kation.
* Elektronaffinitet: Energien ændrer sig, når et atom får en elektron. Høj elektronaffinitet tyder på, at et atom er mere tilbøjelige til at få elektroner og blive en anion.
* Metallig karakter: Metaller har en tendens til at miste elektroner og danne kationer. Ikke-metaller har tendens til at få elektroner og danne anioner.
Usandsynlige parringer:
1. To ikke-metaller med lignende elektronegativitet:
* Eksempel: Nitrogen (N) og ilt (O)
* Forklaring: Begge atomer er meget elektronegative. De er mere tilbøjelige til at dele elektroner i en kovalent binding, men det er usandsynligt at danne en stabil forbindelse med en signifikant forskel i ladning.
2. To metaller:
* Eksempel: Natrium (Na) og Kalium (K)
* Forklaring: Begge metaller har lav ioniseringsenergi og taber let elektroner. De danner ikke let en stabil forbindelse ved at dele elektroner.
3. Et meget elektronegativt ikke-metal og et meget elektropositivt metal:
* Eksempel: Fluor (F) og Francium (Fr)
* Forklaring: Elektronegativitetsforskellen er så stor, at bindingen er meget ionisk. Den resulterende forbindelse ville være ekstremt ustabil og reaktiv.
4. Atomer med fyldte valensskaller:
* Eksempel: Helium (He) og Neon (Ne)
* Forklaring: Begge atomer har en hel oktet af elektroner i deres yderste skal. De er kemisk inerte og danner ikke let bindinger.
Undtagelser:
Selvom disse er generelle retningslinjer, findes der undtagelser. Nogle gange kan usædvanlige forhold eller tilstedeværelsen af andre elementer påvirke sammensætningsdannelsen. For eksempel:
* Ædelgasforbindelser: Mens ædelgasser generelt er inerte, har nogle vist sig at danne forbindelser under ekstreme forhold.
* Intermetalliske forbindelser: Selvom metaller typisk ikke danner forbindelser med hinanden, findes der visse legeringer, hvor metaller danner metalliske bindinger.
Nøglepunkt: Sandsynligheden for, at to atomer danner en forbindelse, er et komplekst samspil af faktorer. Selvom ovenstående principper giver værdifuld vejledning, kræver forudsigelse med sikkerhed en dybere forståelse af de specifikke involverede atomer.
 Varme artikler
Varme artikler
-
 Puster nyt liv i farvesensibiliserede solcellerEt nyt molekylært farvestof forbedrer effektiviteten af solceller. Kredit:Izumi Mindy Takamiya Forskere ved Institute for Integrated Cell-Material Sciences ved Kyoto University har gjort en popu
Puster nyt liv i farvesensibiliserede solcellerEt nyt molekylært farvestof forbedrer effektiviteten af solceller. Kredit:Izumi Mindy Takamiya Forskere ved Institute for Integrated Cell-Material Sciences ved Kyoto University har gjort en popu -
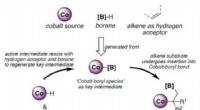 En omkostningseffektiv metode til at syntetisere kemiske byggestenFigur 1:Skematisk, der viser den foreslåede katalytiske vej til syntesen af geminale organodiborforbindelser. Kredit:National University of Singapore NUS-kemikere har udviklet en omkostningseffe
En omkostningseffektiv metode til at syntetisere kemiske byggestenFigur 1:Skematisk, der viser den foreslåede katalytiske vej til syntesen af geminale organodiborforbindelser. Kredit:National University of Singapore NUS-kemikere har udviklet en omkostningseffe -
 Overkommelig katalysator til kuldioxidgenanvendelseKai Junge Puring, Stefan Piontek og Mathias Smialkowski (fra venstre), medlemmer af gruppen ledet af Ulf-Peter Apfel, med elektrolysecellen, hvori forsøgene blev udført. Kredit:RUB, Marquard En ka
Overkommelig katalysator til kuldioxidgenanvendelseKai Junge Puring, Stefan Piontek og Mathias Smialkowski (fra venstre), medlemmer af gruppen ledet af Ulf-Peter Apfel, med elektrolysecellen, hvori forsøgene blev udført. Kredit:RUB, Marquard En ka -
 Elektronisk fast stof kan reducere kulstofemissioner i køleskabe og klimaanlægKredit:CC0 Public Domain En lovende erstatning for de giftige og brandfarlige drivhusgasser, der bruges i de fleste køleskabe og klimaanlæg, er blevet identificeret af forskere fra University of C
Elektronisk fast stof kan reducere kulstofemissioner i køleskabe og klimaanlægKredit:CC0 Public Domain En lovende erstatning for de giftige og brandfarlige drivhusgasser, der bruges i de fleste køleskabe og klimaanlæg, er blevet identificeret af forskere fra University of C
- Hvad loven om bevaringsenergi angiver, der ikke kan oprettes eller ødelægges?
- Forsker finder ud af, at skovfrøer udviklede sig hurtigt som reaktion på vejsalte
- Hvilket stof dannes på overfladen af kobbermetal, når det anbringes i en opløsning sølvnitrat?…
- Hvorfor blev den koniske kolbe ikke vasket med alkali -opløsning, den vil indeholde under titrering…
- Har rock en bestemt form?
- Hvor meget energi kræves for at forårsage en elektron i brintbevægelse fra staten N 3 State 2?


