Kovalente forbindelser og ledningsevne:Udforskning af undtagelserne
Hvorfor mange kovalent bundne molekylære forbindelser er ikke-ledende:
* Ingen frit bevægelige gebyrer: Kovalente bindinger involverer deling af elektroner mellem atomer. Disse elektroner er lokaliseret i bindingen og er ikke frie til at bevæge sig gennem hele forbindelsen. Denne mangel på frit bevægelige ladningsbærere er afgørende for elektrisk ledningsevne.
* Svage intermolekylære kræfter: Molekylære forbindelser holdes typisk sammen af svage intermolekylære kræfter som Van der Waals-kræfter eller hydrogenbinding. Disse kræfter er ikke stærke nok til at tillade overførsel af ladningsbærere.
Undtagelser fra reglen:
* Grafit: Selvom det primært holdes sammen af kovalente bindinger, har grafit en unik struktur med delokaliserede elektroner i dets lag. Disse delokaliserede elektroner kan bevæge sig frit, hvilket gør grafit til en fremragende leder af elektricitet.
* Polymerer: Nogle polymerer, som ledende polymerer, har konjugerede systemer, hvor elektroner kan bevæge sig langs polymerkæden, hvilket resulterer i elektrisk ledningsevne.
* Opløste ioniske forbindelser: Mens kovalente forbindelser i sig selv ofte er ikke-ledende, når de opløses i et opløsningsmiddel som vand, kan nogle dissociere til ioner. Disse ioner kan derefter bære elektrisk strøm.
Opsummering:
Kovalent binding fører generelt til manglende ledningsevne på grund af manglen på frit bevægelige ladninger. Imidlertid kan visse forbindelser, såsom grafit og ledende polymerer, udvise ledningsevne på grund af specifikke strukturelle egenskaber, der tillader ladningsdelokalisering. Derudover kan nogle kovalent bundne forbindelser blive ledende, når de opløses i et opløsningsmiddel, og danner ioner, der kan bære elektrisk strøm.
 Varme artikler
Varme artikler
-
 Kemisk grundlag for papirproduktion:Fra kraftmasse til avanceret blegning og fiberbehandlingerNA/Photos.com/Getty Images Papir fremstår simpelt, men dets fremstilling er afhængig af sofistikeret kemi. Ved at omdanne brune træflis til lyse, alsidige ark fremviser papirindustrien en række præci
Kemisk grundlag for papirproduktion:Fra kraftmasse til avanceret blegning og fiberbehandlingerNA/Photos.com/Getty Images Papir fremstår simpelt, men dets fremstilling er afhængig af sofistikeret kemi. Ved at omdanne brune træflis til lyse, alsidige ark fremviser papirindustrien en række præci -
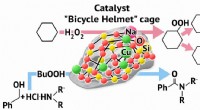 Chemist udvikler en ny katalysator til oxidation og amideringEn RUDN-kemiker udviklede en ny katalysator for oxidation og amidering Kredit:Allen Dressen En RUDN-kemiker har fået en forbindelse med en ny strukturel type, der indeholder atomer af metaller (ko
Chemist udvikler en ny katalysator til oxidation og amideringEn RUDN-kemiker udviklede en ny katalysator for oxidation og amidering Kredit:Allen Dressen En RUDN-kemiker har fået en forbindelse med en ny strukturel type, der indeholder atomer af metaller (ko -
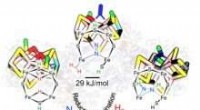 Belyser, hvordan nitrogenase laver ammoniakVandmolekyler bundet tættest på mineralet har en stiv, islignende struktur og kan ikke bevæge sig ind i arrangementer, der muliggør kemiske reaktioner. Vandmolekyler længere fra mineraloverfladen har
Belyser, hvordan nitrogenase laver ammoniakVandmolekyler bundet tættest på mineralet har en stiv, islignende struktur og kan ikke bevæge sig ind i arrangementer, der muliggør kemiske reaktioner. Vandmolekyler længere fra mineraloverfladen har -
 Forskere opdager en grønnere vej til udbredt industrielt materialeKredit:Pixabay/CC0 Public Domain Forskere fra Cardiff University har taget et skridt mod en grønnere, mere bæredygtig måde at skabe et plastmateriale, der findes i en række genstande fra tandbørste
Forskere opdager en grønnere vej til udbredt industrielt materialeKredit:Pixabay/CC0 Public Domain Forskere fra Cardiff University har taget et skridt mod en grønnere, mere bæredygtig måde at skabe et plastmateriale, der findes i en række genstande fra tandbørste
- Celledød:Hvordan et protein driver immunceller til selvmord
- Slår en cinderkegle vulkan voldsomt ud?
- Hvilken slags sten er bjerg?
- Hvad vil der blive gjort, hvis accelerationen af kroppen større, så gravitationsenergi?
- Spontan magnetisering i et ikke-magnetisk interagerende metal
- Archaea har spor til gamle havtemperaturer


