Natrium- og elektrontab:Forståelse af atomstruktur
Her er hvorfor:
* Natriums elektronkonfiguration: Natrium har 11 elektroner. Dens elektronkonfiguration er 2, 8, 1. Den enlige elektron i den yderste skal holdes meget løst.
* Tendens til at miste elektroner: Natrium har en stærk tendens til at miste den enkelte ydre elektron for at opnå en stabil oktet (8 elektroner) i dens yderste skal. Dette gør den mere stabil og ligner ædelgassen Neon.
* Danning af en kation: Når natrium mister en elektron, bliver den til en positivt ladet ion kaldet en natriumkation (Na+).
Sammenfattende er natrium et meget reaktivt metal, der let mister sin yderste elektron for at blive en stabil kation.
 Varme artikler
Varme artikler
-
 Nedbrydelige sukkerbaserede polymerer kan lagre og frigive nyttig molekylær fragtKredit:CC0 Public Domain Nedbrydeligt, biobaserede polymerer tilbyder muligheder for kemisk genbrug, og de kan være et redskab til at lagre og frigive nyttige molekyler. Forskere har udviklet en k
Nedbrydelige sukkerbaserede polymerer kan lagre og frigive nyttig molekylær fragtKredit:CC0 Public Domain Nedbrydeligt, biobaserede polymerer tilbyder muligheder for kemisk genbrug, og de kan være et redskab til at lagre og frigive nyttige molekyler. Forskere har udviklet en k -
 Forskere finder nye måder at bruge bioraffinaderikemikalier påSkræddersyede designerbakterier som fremtidige værktøjer i valoriseringen af bioraffinaderi-furaner. Kredit:Jan Deska Forskere fra gruppen Synthetic Organic Chemistry ved Aalto Universitet har e
Forskere finder nye måder at bruge bioraffinaderikemikalier påSkræddersyede designerbakterier som fremtidige værktøjer i valoriseringen af bioraffinaderi-furaner. Kredit:Jan Deska Forskere fra gruppen Synthetic Organic Chemistry ved Aalto Universitet har e -
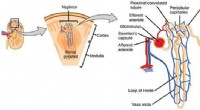 Enhed til at fremskynde opdagelse af lægemidler til nyresygdommeKredit:CNX OpenStax Forskere fra Institut for Ingeniørvidenskab samarbejder med industrien og den akademiske verden om at udvikle et apparat til at forbedre testningen af lægemidler til nyresygd
Enhed til at fremskynde opdagelse af lægemidler til nyresygdommeKredit:CNX OpenStax Forskere fra Institut for Ingeniørvidenskab samarbejder med industrien og den akademiske verden om at udvikle et apparat til at forbedre testningen af lægemidler til nyresygd -
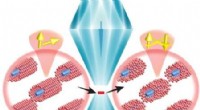 Forskere opdager superleder med uventet gitterkonfigurationKombination af langtrækkende ordnede og kortdistance uordnede strukturer på atomniveau er demonstreret i tryksat Q1D (TaSe4)2I, hvor der også observeres en kondensering af Cooper-par. Kredit:ZHANG Guf
Forskere opdager superleder med uventet gitterkonfigurationKombination af langtrækkende ordnede og kortdistance uordnede strukturer på atomniveau er demonstreret i tryksat Q1D (TaSe4)2I, hvor der også observeres en kondensering af Cooper-par. Kredit:ZHANG Guf
- Forskellen mellem varme og kolde molekyler
- Hvorfor er ikke vedvarende energi blevet brugt så meget indtil nu?
- Hvordan måler du brosikkerhed? Godt kryds den, når vi kommer til det
- Stigende temperaturer ændrer, hvornår og hvor meget folk kommer ud på offentlige arealer
- Hvilket af følgende er et syre-ammoniak-kaliumhydroxid svovlsyrelithiumhydroxid?
- Tidsoverførselsydelsen for BDS-3-satellitter blev forbedret


