Aktive metaller:egenskaber, eksempler og reaktivitet - [dit brand/dit websted]
Her er nogle nøgleegenskaber ved aktive metaller:
* Høj reaktivitet: De reagerer let med andre grundstoffer, især ikke-metaller som oxygen, halogener og syrer.
* Lav ioniseringsenergi: De mister let elektroner for at danne kationer, fordi deres yderste elektroner er løst bundet.
* Stærke reduktionsmidler: De donerer elektroner til andre stoffer, hvilket får dem til at blive reduceret.
Eksempler på aktive metaller:
* Lithium (Li), Natrium (Na), Kalium (K): Alkalimetaller er den mest reaktive gruppe.
* Magnesium (Mg), Calcium (Ca), Barium (Ba): Jordalkalimetaller er også meget reaktive, dog lidt mindre end alkalimetaller.
* Aluminium (Al): Selvom det ikke er så reaktivt som alkali- og jordalkalimetaller, betragtes aluminium stadig som et aktivt metal.
Reaktioner af aktive metaller:
* Reaktion med oxygen: De danner oxider ved reaktion med oxygen. For eksempel reagerer natrium kraftigt med oxygen til dannelse af natriumoxid (Na2O).
* Reaktion med vand: De reagerer med vand for at producere brintgas og et metalhydroxid. For eksempel reagerer kalium voldsomt med vand for at producere kaliumhydroxid (KOH) og brintgas (H2).
* Reaktion med syrer: De reagerer med syrer for at producere brintgas og et salt. For eksempel reagerer magnesium med saltsyre og danner magnesiumchlorid (MgCl2) og hydrogengas (H2).
Anvendelser af aktive metaller:
* Batterier: Aktive metaller som lithium bruges i batterier på grund af deres høje reaktivitet og evne til let at donere elektroner.
* Reduktionsmidler: Aktive metaller bruges som reduktionsmiddel i forskellige kemiske processer.
* Legeringer: Aktive metaller bruges ofte i legeringer for at bibringe specifikke egenskaber, såsom styrke og korrosionsbestandighed.
Bemærk: Aktive metaller opbevares generelt i inerte atmosfærer eller under olie for at forhindre dem i at reagere med ilt og fugt.
Sidste artikelNatrium- og elektrontab:Forståelse af atomstruktur
Næste artikelIoniske vs. kovalente bindinger i salpetersyre (HNO₃)
 Varme artikler
Varme artikler
-
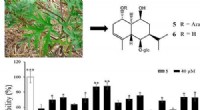 Ambrosie-forbindelser kunne beskytte nerveceller mod AlzheimersKredit:American Chemical Society Når foråret kommer på den nordlige halvkugle, mange mennesker forbander ragweed, en primær synder i sæsonbestemte allergier. Men videnskabsmænd har måske opdaget e
Ambrosie-forbindelser kunne beskytte nerveceller mod AlzheimersKredit:American Chemical Society Når foråret kommer på den nordlige halvkugle, mange mennesker forbander ragweed, en primær synder i sæsonbestemte allergier. Men videnskabsmænd har måske opdaget e -
 Fordel:Vand - Forskere løser nøglespørgsmål om titaniumoxid, vand interaktionerNår vand (vist med blåt) kommer ind for en landing på den almindelige katalysator titaniumoxid (vist med rødt og grønt), det deler sig i hydroxyler (på venstre overflade) lige under halvdelen af tid
Fordel:Vand - Forskere løser nøglespørgsmål om titaniumoxid, vand interaktionerNår vand (vist med blåt) kommer ind for en landing på den almindelige katalysator titaniumoxid (vist med rødt og grønt), det deler sig i hydroxyler (på venstre overflade) lige under halvdelen af tid -
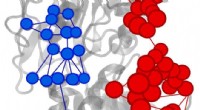 Kemikere finder et nyt værktøj til at forstå enzymer – GoogleEffektorudløst stigning (rød) eller reduktion (blå) af informationsstrømmen i IGPS-enzym. Kredit:Uriel Morzan Yale-forskere har taget en ny tilgang til at optrevle den komplekse struktur og regule
Kemikere finder et nyt værktøj til at forstå enzymer – GoogleEffektorudløst stigning (rød) eller reduktion (blå) af informationsstrømmen i IGPS-enzym. Kredit:Uriel Morzan Yale-forskere har taget en ny tilgang til at optrevle den komplekse struktur og regule -
 Kaffe-ring effekt udnyttet til at give hurtig, lavprisanalyse af postevandPostevandsdråber fra to bygninger på Michigan State University campus efterlader forskellige kafferingmønstre; hårdt vand vises til venstre, og vand behandlet med et blødgøringsmiddel er vist til højr
Kaffe-ring effekt udnyttet til at give hurtig, lavprisanalyse af postevandPostevandsdråber fra to bygninger på Michigan State University campus efterlader forskellige kafferingmønstre; hårdt vand vises til venstre, og vand behandlet med et blødgøringsmiddel er vist til højr
- Bare tilsæt (kappe)vand:Ny forskning knækker mysteriet om, hvordan de første kontinenter blev til…
- Hvorfor siger vi, at hastighed er en vektor og hastighed ikke vektor?
- Hvorfor er indisk astronomi vigtig i Indien?
- Video:Er vi ved at løbe tør for vanilje?
- Ledning forekommer lettere mellem faste stoffer og væsker. Dette skyldes, at partiklerne i gasser e…
- Er Mount Kilimanjaro på vestkysten af Australien?


