Ferrihydroxidopløselighed:Forståelse af den optimale pH
* Fe(OH)₃ er en svag base: Det reagerer med syrer og danner opløselige salte.
* Le Chateliers princip: Når en syre tilsættes, reagerer den med hydroxidionerne (OH-) fra Fe(OH)3. Denne reaktion forskyder ligevægten for at begunstige opløsningen af mere Fe(OH)3 for at erstatte de forbrugte OH-ioner.
Eksempel:
Fe(OH)3(s) + 3H+(vandig) ⇌ Fe3+(vandig) + 3H2O(l)
Ved at tilsætte en stærk syre som HCl, vil H⁺-ionerne reagere med OH⁻-ionerne, hvilket driver ligevægten til højre, hvilket øger opløseligheden af Fe(OH)3.
Vigtig bemærkning: Mens sure opløsninger øger opløseligheden, kan ekstrem høj surhedsgrad føre til dannelsen af andre komplekser, som kan mindske opløseligheden af Fe(OH)3.
 Varme artikler
Varme artikler
-
 Fra identifikation til et kemisk fingeraftryk for sprængstoffer i retsmedicinsk forskningCobra fyrværkeri. Kredit:Karlijn Bezemer Politiet støder ofte på sprængstoffer i deres retsmedicinske efterforskninger relateret til kriminelle og terroraktiviteter. Kemisk analyse af sprængstoffe
Fra identifikation til et kemisk fingeraftryk for sprængstoffer i retsmedicinsk forskningCobra fyrværkeri. Kredit:Karlijn Bezemer Politiet støder ofte på sprængstoffer i deres retsmedicinske efterforskninger relateret til kriminelle og terroraktiviteter. Kemisk analyse af sprængstoffe -
 Flydende platin ved stuetemperatur:Den seje katalysator for en bæredygtig revolution inden for indu…Flydende gallium- og platinperler tæt på. Kredit:Dr. Md. Arifur Rahim, UNSW Sydney. Forskere i Australien har været i stand til at bruge spormængder af flydende platin til at skabe billige og højef
Flydende platin ved stuetemperatur:Den seje katalysator for en bæredygtig revolution inden for indu…Flydende gallium- og platinperler tæt på. Kredit:Dr. Md. Arifur Rahim, UNSW Sydney. Forskere i Australien har været i stand til at bruge spormængder af flydende platin til at skabe billige og højef -
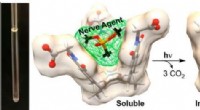 Indfangning af giftige forbindelser med molekylære kurveKredit:Ohio State University Forskere har udviklet designermolekyler, som måske en dag kan opsøge og fange dødelige nervestoffer og andre giftige forbindelser i miljøet – og muligvis i mennesker.
Indfangning af giftige forbindelser med molekylære kurveKredit:Ohio State University Forskere har udviklet designermolekyler, som måske en dag kan opsøge og fange dødelige nervestoffer og andre giftige forbindelser i miljøet – og muligvis i mennesker. -
 Polymermembraner kunne have fordel af at tage en dukkertI forsøget, forskere dykkede først en hydrofob polymer membran i garvesyre (TA), en almindelig polyfenol. Derefter, den tørrede TA dip-coatede membran fyldes i atomlagsaflejringsreaktoren (ALD) til ov
Polymermembraner kunne have fordel af at tage en dukkertI forsøget, forskere dykkede først en hydrofob polymer membran i garvesyre (TA), en almindelig polyfenol. Derefter, den tørrede TA dip-coatede membran fyldes i atomlagsaflejringsreaktoren (ALD) til ov
- Opstår der foldede bjerge ved at plader skubbes ned?
- Mammoth felt fyrer op i Norges olieindustri
- Satellitobservationer forbedrer jordskælvsovervågning, respons
- Hvilken flydende kraft af modsætter løft?
- Hvordan bestemmer du antallet af subatomære partikler i et atom baseret på dets identitet?
- Skal vi droppe store eksamenssale? Forskning viser, hvordan højt til loftet er forbundet med en lav…


